题目内容
3.利用硫铁矿(主要成分FeS2)生产硫酸和绿矾(FeSO4•7H2O)的工业流程示意图如图: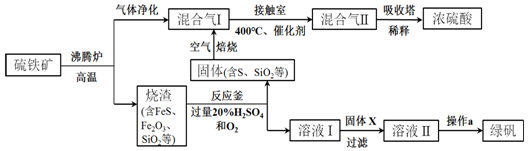
(1)沸腾炉中,硫铁矿进行粉碎处理的目的是增大反应物的接触面积,提高化学反应速率.
(2)接触室中,发生的主要反应是SO2与O2的反应,其化学方程式是2SO2+O2$?_{△}^{催化剂}$2SO3.
(3)反应釜中,烧渣经过反应转化为溶液I和固体.
①烧渣中的FeS在反应中做还原剂(填“氧化”或“还原”).
②溶液I中所含溶质的化学式是Fe2(SO4)3、H2SO4.
(4)操作a的主要步骤是:加热浓缩、冷却结晶、过滤洗涤.
(5)流程中,固体X可以选择硫铁矿(FeS2)或Fe;当固体X为硫铁矿(FeS2)时,将溶液I与固体X发生反应的离子方程式补充完整:
FeS2+14Fe3++8H2O═Fe2++SO42-+16H+.
分析 硫铁矿在沸腾炉中高温生成氧化铁与二氧化硫,混合气体Ⅰ为二氧化硫和空气,经过接触室后二氧化硫被氧化成三氧化硫,所以混合气体Ⅱ为三氧化硫、二氧化硫、空气等,沸腾炉中产生的炉渣主要为硫化亚铁、氧化铁、二氧化硅等,加入硫酸溶解,再用氧气氧化可得溶液Ⅰ主要成分为硫酸铁,硫酸铁中加入铁粉得溶液Ⅱ为硫酸亚铁溶液,经蒸发浓缩、冷却结晶得到硫酸亚铁晶体,烧渣用酸溶解后得固体主要成分为二氧化硅和硫,硫经氧化得二氧化硫,可循环利用,
(1)固体粉碎处理可使固体与气体充分接触,加快反应速率;
(2)接触室中,SO2与O2的反应生成SO3;
(3)①反应釜中的FeS被氧化成硫,据此答题;
②根据上面的分析可知,溶液Ⅰ主要成分为硫酸铁及过量的硫酸;
(4)操作a为从硫酸亚铁溶液中获得硫酸亚铁晶体,可以用降温结晶的方法;
(5)流程中,固体X主要目的是将铁离子还原成亚铁离子,据此书写离子方程式.
解答 解:(1)沸腾炉中,硫铁矿进行粉碎处理的目的是使固体与气体充分接触,加快反应速率,
故答案为:增大反应物的接触面积,提高化学反应速率;
(2)接触室中,SO2与O2的反应生成SO3,反应的化学方程式为2SO2+O2 $?_{△}^{催化剂}$ 2SO3,
故答案为:2SO2+O2 $?_{△}^{催化剂}$ 2SO3;
(3)①反应釜中的FeS被氧化成硫,所以FeS在反应中做还原剂,
故答案为:还原;
②根据上面的分析可知,溶液Ⅰ主要成分为硫酸铁及过量的硫酸,其化学式为Fe2(SO4)3、H2SO4,
故答案为:Fe2(SO4)3、H2SO4;
(4)操作a为从硫酸亚铁溶液中获得硫酸亚铁晶体,其操作为加热浓缩、冷却结晶、过滤洗涤,
故答案为:冷却结晶;
(5)流程中,固体X主要目的是将铁离子还原成亚铁离子,所以X可以是FeS2或Fe,硫铁矿(FeS2)与硫酸铁发生氧化还原反应生成亚铁离子和硫酸根离子,反应的离子方程式为FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+,
故答案为:Fe;14Fe3+、8H2O、16H+.
点评 本题考查制备方案设计,侧重考查学生对操作步骤、原理的分析评价,是对学生综合能力的考查,难度中等.

| A. | 2mol•L-1 | B. | 1.6mol•L-1 | C. | 0.8mol•L-1 | D. | 0.4mol•L-1 |
 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C分别充入等质量的X、H2、Y三种气体.当隔板静止时,A、C内的气体密度相等,下列说法不正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C分别充入等质量的X、H2、Y三种气体.当隔板静止时,A、C内的气体密度相等,下列说法不正确的是( )| A. | 摩尔质量:M(X)=M(Y) | B. | 分子的数目:N (X)=N(Y) | ||
| C. | 气体的体积:V(X)=V(Y) | D. | 物质的质量:m(X)<n(H2)<n(Y) |
| A. | ②中水的电离程度的是①的8倍 | |
| B. | ①和③中水的电离程度相等 | |
| C. | 等体积的①和④混合后所得溶液中:c(NH3•H2O)<c(NH4+) | |
| D. | ②中水的电离程度等于④ |