题目内容
一定温度下,将3mol A气体和1mol B气体通过一密闭容器中,发生如下反应:3A(g)+B(g)═xC(g).若容器体积固定为2L,反应2min后达到平衡状态,测得剩余1.8mol A,C的浓度为0.4mol/L.求:
①B的平均反应速率;②x的值;③A的转化率;④化学平衡常数.
①B的平均反应速率;②x的值;③A的转化率;④化学平衡常数.
考点:化学平衡的计算
专题:化学平衡专题
分析:利用三段式法计算 3A(g)+B(g)═xC(g)
起始(mol/L):1.5 0.5 0
转化(mol/L):0.6 0.2 0.2x
平衡(mol/L):0.9 0.3 0.2x
0.2x=0.4,x=2,以此解答该题.
起始(mol/L):1.5 0.5 0
转化(mol/L):0.6 0.2 0.2x
平衡(mol/L):0.9 0.3 0.2x
0.2x=0.4,x=2,以此解答该题.
解答:
解:利用三段式法计算 3A(g)+B(g)═xC(g)
起始(mol/L):1.5 0.5 0
转化(mol/L):0.6 0.2 0.2x
平衡(mol/L):0.9 0.3 0.2x
①B的平均反应速率=
=0.1mol/L?min,答:B的平均反应速率为0.1mol/L?min;
②依据计算得到,0.2x=0.4,x=2,答:x的值为2;
③A的转化率=
×100%=40%,答:B的平均反应速率为40%;
④化学平衡常数K=
=0.73,答:反应的平衡常数为0.73.
起始(mol/L):1.5 0.5 0
转化(mol/L):0.6 0.2 0.2x
平衡(mol/L):0.9 0.3 0.2x
①B的平均反应速率=
| 0.2mol/L |
| 2min |
②依据计算得到,0.2x=0.4,x=2,答:x的值为2;
③A的转化率=
| 0.6mol/L |
| 1.5mol/L |
④化学平衡常数K=
| 0.42 |
| 0.93×0.3 |
点评:本题考查了化学平衡计算的分析应用,主要是反应速率、转化率、平衡常数的概念计算,掌握基础是关键,题目难度中等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
 某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位.阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位.阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是( )| A、1:8 | B、1:4 |
| C、1:2 | D、1:1 |
下列各离子或分子组能在水溶液中大量共存的是( )
| A、NH4+、H+、NO3-、Fe2+ |
| B、Fe3+、ClO-、Na+、AlO2- |
| C、CO32-、SO32-、Na+、Ba2+ |
| D、SO42-、Cl-、Na+、Al3+ |
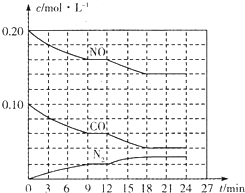 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
 中的手性碳原子
中的手性碳原子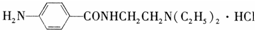 )俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
)俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
