题目内容
把湿润的蓝色石蕊试纸放入盛有Cl2的集气瓶中,下面对所能观察到的现象描述正确的是( )
| A、变红 | B、先变红后变白 |
| C、变成无色 | D、不变色 |
考点:氯气的化学性质
专题:卤族元素
分析:把湿润的蓝色石蕊试纸放入盛有Cl2的集气瓶中,氯气与水反应生成HCl、HClO,HCl具有酸性,HClO具有漂白性,以此来解答.
解答:
解:把湿润的蓝色石蕊试纸放入盛有Cl2的集气瓶中,氯气与水反应生成HCl、HClO,HCl具有酸性,HClO具有漂白性,则观察到湿润的蓝色石蕊试纸先变红后褪色,
故选B.
故选B.
点评:本题考查氯气的化学性质,为高频考点,把握氯气与水的反应及产物的性质为解答的关键,注意物质的性质及HClO具有漂白性,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在不同条件下,分别测得反应2SO2+O2?2SO3的化学反应速率,其中表示该反应进行得最快的是( )
| A、ν(SO2)=4mol/(L?min) |
| B、ν(O2)=3 mol/(L?min) |
| C、ν(SO2)=0.1 mol/(L?s) |
| D、ν(SO3)=0.2mol/(L?s) |
下列物质能使湿润的有色布条褪色的是( )
| A、氯化钙 | B、氯化氢 |
| C、氯气 | D、氯化钠 |
新产品“不粘锅”受到广大群众的欢迎,其生产工艺十分简单:在金属锅的内壁上涂一层聚四氟乙烯.下列说法中正确的是( )
| A、聚四氟乙烯的结构简式是:F2C=CF2 |
| B、聚四氟乙烯中含碳,所以在加热时能够燃烧生成二氧化碳 |
| C、由于C-C键和F-C键很牢固,因而聚四氟乙烯的性质稳定,在使用时不会污染食物 |
| D、聚四氟乙烯中不能与常见的氧化剂接触,防止被氧化 |
下列高聚物中,由两种不同的单体通过缩聚反应制得的是( )
A、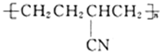 |
B、 |
C、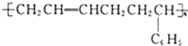 |
D、 |
下列说法正确的是( )
| A、甲烷和乙烯都可以与氯气反应 |
| B、乙炔可以与氢气发生加成反应,苯不能与氢气加成 |
| C、除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离 |
| D、高锰酸钾可以氧化苯和甲烷 |
已知25℃时有关物质的电离平衡常数:
下列叙述错误的是( )
| 弱酸 | CH3COOH | 苯酚 | H2CO3 |
| 电离平衡常数 | 1.75×l0-5 | 1.1×l0-10 | K1=4.4×l0-7 K2=4.7×l0-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) |
| B、向苯酚钠溶液中通入少量CO2气体反应为:C6H5O-+H2O+CO2→C6H5OH+HCO3- |
| C、等物质的量浓度的苯酚稀溶液与NaOH稀溶液等体积混合后溶液中:c(Na+)>c(C6H5O-)>c(OH-)>c(H+) |
| D、NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
下列有关说法正确的是( )
| A、CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0 |
| B、放热反应的反应速率总是大于吸热反应的反应速率 |
| C、N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 |
| D、液氨是一种重要的制冷剂,说明氨气在液化时吸收大量的热 |
下列材料都具有一定的特殊性能,其中是由主族元素和副族元素形成的是( )
| A、透明陶瓷材料硒化锌 |
| B、超导材料K3C60 |
| C、半导体材料砷化镓 |
| D、吸氢材料镧镍合金 |