题目内容
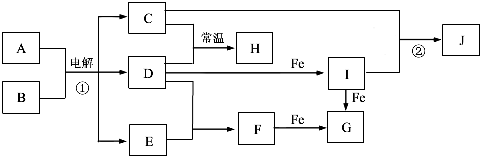
(根据下列反应框图填空,已知反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化合物E的反应.

(1)单质L是 . (2)化合物B是 .
(3)图中除反应①以外,还有两个用于工业生产的反应,是 和 (填代号).它们的化学反应方程式分别是 和 .

(1)单质L是
(3)图中除反应①以外,还有两个用于工业生产的反应,是
考点:无机物的推断
专题:推断题
分析:由题意可知,反应①是工业上生产化合物D的反应,考虑是高温分解石灰石的反应,再由⑤是实验室鉴定E的反应,结合转化关系,C为CaCO3,D为CaO,E为CO2,G为Ca(OH)2,B为H2O.则反应②是电解饱和食盐水:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,则A为NaCl,产物中只有Cl2能够与Ca(OH)2反应,故H为Cl2,则单质L为H2,④为制漂白粉的反应,方程式为2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,结合物质的相关性质以及题目要求可解答该题.
| ||
解答:
解:由题意可知,反应①是工业上生产化合物D的反应,考虑是高温分解石灰石的反应,再由⑤是实验室鉴定E的反应,结合转化关系,C为CaCO3,D为CaO,E为CO2,G为Ca(OH)2,B为H2O.则反应②是电解饱和食盐水:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,则A为NaCl,产物中只有Cl2能够与Ca(OH)2反应,故H为Cl2,则单质L为H2,④为制漂白粉的反应,方程式为2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O,
(1)由以上分析可知,L为H2,故答案为:H2;
(2)由上述分析可知,化合物BH2O,故答案为:H2O;
(3)反应②是电解饱和食盐水,方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,④为制漂白粉的反应,
方程式为2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O,
故答案为:②;④;2NaCl+2H2O
2NaOH+H2↑+Cl2↑;2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O.
| ||
(1)由以上分析可知,L为H2,故答案为:H2;
(2)由上述分析可知,化合物BH2O,故答案为:H2O;
(3)反应②是电解饱和食盐水,方程式为2NaCl+2H2O
| ||
方程式为2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O,
故答案为:②;④;2NaCl+2H2O
| ||
点评:本题考查无机物推断,难度中等,综合考查元素化合物知识,注意充分利用反应条件等信息是推断“突破口”,注意中学常见工业生产.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学与生活、社会密切相关.下列说法错误的是( )
| A、发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统 |
| B、含磷洗衣粉中的磷是植物生长的营养元素,洗衣水可排入河泊 |
| C、在入海口的钢铁闸门上装一定数量的锌块可防止闸门被腐蚀 |
| D、国家规定商家不得无偿提供塑料袋,是为了减少白色污染 |
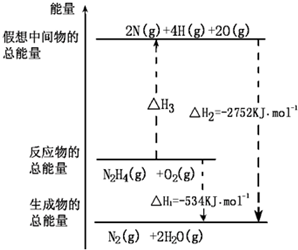 肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图,已知断裂1mol化学键所需的能量(kJ):N≡N为942、N-H为391、O=O为500,则断裂1molN-N键所需的能量(kJ)是( )
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图,已知断裂1mol化学键所需的能量(kJ):N≡N为942、N-H为391、O=O为500,则断裂1molN-N键所需的能量(kJ)是( )| A、1327 | B、391 |
| C、516 | D、154 |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:方案一:铜铝混合物
测定生成气体的体积方案二:铜铝混合物
测定剩余固体的质量下列有关判断中不正确的是( )
| 足量溶液A |
| 充分反应 |
| 足量溶液B |
| 充分反应 |
| A、溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B、方案一可能产生氢气,方案二可能剩余铜 |
| C、若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| D、实验室中方案Ⅱ更便于实施 |
下列各组实验中溶液最先变浑浊的是( )
| A、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度10℃ |
| B、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度10℃ |
| C、0.1 mol/L Na2S2O3和H2SO4各5 mL,加水5 mL,反应温度30℃ |
| D、0.2 mol/L Na2S2O3和H2SO4各5 mL,加水10 mL,反应温度30℃ |
对于可逆反应A(g)+B(g)?C(g)△H<0,下列图象正确的是( )
A、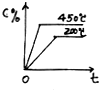 |
B、 |
C、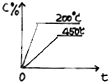 |
D、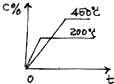 |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| C、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| D、在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:Fe3+、NH4+、H+ |