题目内容
3.下列混合物无论总质量或总物质的量一定,完全燃烧生成二氧化碳、水的量都一定的是( )| A. | 甲烷和甲醇 | B. | 丙醛和丙酮 | C. | 乙烯和乙炔 | D. | 乙烯和乙醇 |
分析 混合物无论总质量或总物质的量一定,完全燃烧生成二氧化碳、水的量都一定,说明二者的分子式相同,据此分析解答.
解答 解:混合物无论总质量或总物,质的量一定,完全燃烧生成二氧化碳、水的量都一定,说明二者的分子式相同,甲烷和甲醇、乙烯和乙炔、乙烯和乙醇的分子式都分别不相同,只有丙酮、丙醛的分子式相同,故选B.
点评 本题考查混合物的计算,为高频考点,侧重考查学生分析判断能力,明确题给信息含义是解本题关键,如果是总质量一定,完全燃烧生成二氧化碳、水的量一定时,两种有机物的最简式应该相同,题目难度不大.

练习册系列答案
相关题目
13.NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 14g乙烯与14g苯含有的氢原子数均为2NA | |
| B. | 0.1molFe3+与足量的HI溶液反应,转移的电子数为0.1NA | |
| C. | 1L0.1mol•L-1NaHS溶液中,HS-与H2S数目之和为0.1NA | |
| D. | 6.4g铜溶于30mL10mol•L-1硝酸中,产生气体的分子数为0.2NA |
14.下列离子方程式中,正确的是( )
| A. | 盐酸与氨水混合:H++OH-═H2O | |
| B. | 金属钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 碳酸钠与过量稀盐酸:CO32-+2H+═CO2↑+H2O | |
| D. | 氯气与碘化钾溶液的反应:Cl2+I-=I2+Cl- |
11.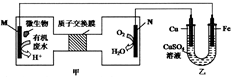 下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
 下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )
下列装置由甲、乙部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)NH2]氧化为环境友好物质形成的化学电源.当电池工作时,下列说法错误的是( )| A. | 甲中H+透过质子交换膜由左向右移动 | |
| B. | M极电极反应式:H2N(CH2)NH2+4H2O-16e-═2CO2↑+N2↑+16e- | |
| C. | 一段时间后,乙中CuSO4溶液浓度基本保持不变 | |
| D. | 当N极消耗0.25molO2时,则铁极增重16g |
18.将两个铂电极用导线连接,放置在NaOH溶液中,然后向两极分别通入甲烷和氧气,下列叙述正确的是( )
| A. | 正极反应式为O2+4e-═2O2- | |
| B. | 放电时溶液中的阳离子向正极方向移动 | |
| C. | 该电池反应为CH4+2O2═CO2+2H2O | |
| D. | 通入CH4一极的电极反应式为CH4+2O2+8e-═CO2+2H2O |
8.某实验小组为测定某石灰石中CaCO3的质量分数,先称取W g石灰石样品,加入过量的浓度为6mol•L-1的盐酸,使样品完全溶解,加热煮沸后,除去溶解的CO2,再向溶液中加入足量的草酸铵[(NH4)2C2O4]溶液后,慢慢加入氨水降低溶液的酸度,则析出草酸钙沉淀:C2O42-+Ca2+=CaC2O4↓,过滤出CaC2O4后,用稀H2SO4溶解:CaC2O4+H2SO4=H2C2O4+CaSO4,再用蒸馏水稀释溶液至V0 mL.取出V1 mL,用a mol•L-1的KMnO4酸性溶液进行滴定,此时发生反应:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,若滴定终点时消耗a mol•L-1的KMnO4溶液V2 mL,则样品中CaCO3的质量分数为( )
| A. | $\frac{25a{V}_{0}{V}_{2}}{W{V}_{1}}$% | B. | $\frac{25a{V}_{1}{V}_{2}}{W{V}_{0}}$% | C. | $\frac{25a{V}_{1}{V}_{0}}{W{V}_{2}}$% | D. | $\frac{25a{V}_{2}}{W}$% |
15.滴定分析法按反应类型一般可以分为__类.( )
| A. | 二 | B. | 一 | C. | 四 | D. | 三 |
12.下列除去杂质(括号的物质为杂质)的方法中,正确的是( )
| A. | FeCl2溶液(FeCl3):加入过量Cu后过滤 | |
| B. | Na2CO3固体(NaHCO3):加热 | |
| C. | CH3COOCH2CH3(CH3COOH):加NaOH溶液后振荡、分液 | |
| D. | Cl2(HCl):通过NaOH溶液后干燥 |
16.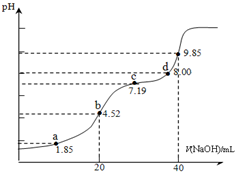 已知:pKa=-lgKa,25℃时,H2SO3的 pKa1=1.85,pKa2=7.19.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2SO3的 pKa1=1.85,pKa2=7.19.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH).下列说法不正确的是( )
 已知:pKa=-lgKa,25℃时,H2SO3的 pKa1=1.85,pKa2=7.19.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-lgKa,25℃时,H2SO3的 pKa1=1.85,pKa2=7.19.用0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH).下列说法不正确的是( )| A. | a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1 mol•L-1 | |
| B. | b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | |
| C. | c点所得溶液中:c(Na+)>3c(HSO3-) | |
| D. | d点所得溶液中:c(Na+)>c(SO32-)>c(HSO3-) |