题目内容
化工行业的发展必须符合国家节能减排的总体要求.如图是煤化工产业链的一部分,试运用所学知识,解决下列问题:
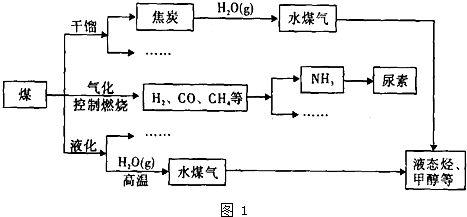
(1)如图中有一个反应是德国化学家哈伯进行过的实验,农业生产是该反应最大的应用领域.该反应的△H<O,则该反应的△S 0(填“>”或“<”)
(2)已知在一定温度下,以下三个反应的平衡常数为K1、K2、K3
①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
则K1、K2、K3之间的关系是 .
(3)二甲醚是一种重要的清洁燃料,工业上可利用煤的气化产物(水煤气)合成二甲醚.利用水煤气合成=甲醚的热化学方程式为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1
①该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是 (填字母代号).
a.降低温度 b.缩小容器体积 c.加入催化剂 d.增加H2的浓度e.分离出二甲醚
②已知:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-42kJ?mol-1某些化学键的键能数据如下表
 CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是 kJ?mol-1.
CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是 kJ?mol-1.
(4)二甲醚也可以通过CH3OH分子间脱水制得
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
已知在280℃,体积不变的密闭容器中进行上述反应,t2时达到平衡,各组分起始和平衡浓度见下表.
①表中c1= .在t2min内平均反应速率v(H2O)= .
②若在400℃,相同的密闭容器中进行上述反应,请在F图中画出CH3OCH3浓度随时问变化的关系图.

(1)如图中有一个反应是德国化学家哈伯进行过的实验,农业生产是该反应最大的应用领域.该反应的△H<O,则该反应的△S
(2)已知在一定温度下,以下三个反应的平衡常数为K1、K2、K3
①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
则K1、K2、K3之间的关系是
(3)二甲醚是一种重要的清洁燃料,工业上可利用煤的气化产物(水煤气)合成二甲醚.利用水煤气合成=甲醚的热化学方程式为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-274kJ?mol-1
①该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,可以采取的措施是
a.降低温度 b.缩小容器体积 c.加入催化剂 d.增加H2的浓度e.分离出二甲醚
②已知:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-42kJ?mol-1某些化学键的键能数据如下表
| 化学键 | C-H | H-O | H-H | C-O | C=O |
| 键能/KJ mol-1 | 413 | 463 | 436 | 358 | 802 |
 CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是
CO中的C与O之间为叁键连接,则CO中碳氧叁键的键能是(4)二甲醚也可以通过CH3OH分子间脱水制得
2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1
已知在280℃,体积不变的密闭容器中进行上述反应,t2时达到平衡,各组分起始和平衡浓度见下表.
| CH3OH(g) | CH3OCH3(g) | H2O(g) | |
| 起始浓度/mol?L-1 | 2.00 | 0.50 | 0 |
| 平衡浓度/mol?L-1 | c1 | 1.00 | c2 |
②若在400℃,相同的密闭容器中进行上述反应,请在F图中画出CH3OCH3浓度随时问变化的关系图.
考点:化学平衡的计算,反应热和焓变,化学平衡建立的过程,化学平衡的影响因素
专题:
分析:(1)德国化学家哈伯发明了直接合成氨法,合成氨的化学方程式为N2+3H2?2NH3,反应前后气体物质的量减少,因此△S<0;
(2)已知①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
可得关系式③=①+②,因此K3=K1×K2;
(3)①根据外加条件对速率和平衡的影响分析;
②根据△H=反应物的键能总和-生成物的键能总和计算CO中碳氧叁键的键能;
(4)①
=
计算,v(H2O)=v(CH3OCH3)=
=
mol/(L?min);
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1,温度升高,化学反应速率加快,达到平衡的时间小于t2,平衡逆向移动,达到平衡时,CH3OCH3浓度小于1.00mol/L,以此作图.
(2)已知①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
可得关系式③=①+②,因此K3=K1×K2;
(3)①根据外加条件对速率和平衡的影响分析;
②根据△H=反应物的键能总和-生成物的键能总和计算CO中碳氧叁键的键能;
(4)①
| (1.00-0.50)mol/L |
| 2.00mol/L-c1 |
| 1 |
| 2 |
| (1.00-0.50)mol/L |
| t2min |
| 0.5 |
| t2 |
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1,温度升高,化学反应速率加快,达到平衡的时间小于t2,平衡逆向移动,达到平衡时,CH3OCH3浓度小于1.00mol/L,以此作图.
解答:
解:(1)德国化学家哈伯发明了直接合成氨法,合成氨的化学方程式为N2+3H2?2NH3,反应前后气体物质的量减少,因此△S<0,
故答案为:<;
(2)已知①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
可得关系式③=①+②,因此K3=K1×K2;
故答案为:K3=K1×K2;
(3)①该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,则速率加快而且平衡正移;
A.降低温度,反应速率减小,不符合题意,故a不选;
B.缩小容器体积,压强增大,速率加快,平衡正移二甲醚的产率提高,故b选;
C.加入催化剂,速率加快,但是平衡不移动,不符合题意,故c不选;
D.增加H2的浓度,速率加快,平衡正移二甲醚的产率提高,故d选;
E.分离出二甲醚,浓度减小,反应速率减小,不符合题意,故e不选;
故答案为:bd;
②CO(g)+H2O(g)=CO2(g)+H2(g)△H=-42 kJ?mol-1,由△H=反应物的键能总和-生成物的键能总和可得:
EC≡O+2×463kJ?mol-1-(2×802kJ?mol-1+436kJ?mol-1)=-42 kJ?mol-1,
解得:EC≡O=1072 kJ?mol-1,
故答案为:1072;
(4)①
=
,解得c1=1.00mol/L,v(H2O)=v(CH3OCH3)=
=
mol/(L?min);
故答案为:1.00;
mol/(L?min);
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1,温度升高,化学反应速率加快,达到平衡的时间小于t2,平衡逆向移动,达到平衡时,CH3OCH3浓度小于1.00mol/L,CH3OCH3浓度随时问变化的关系图为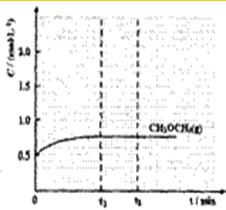 ,故答案为:
,故答案为: .
.
故答案为:<;
(2)已知①C(s)+CO2(g)?2CO(g) K1;
②CO(g)+H2O(g)?H2(g)+CO2(g) K2;
③C(s)+H2O(g)?CO(g)+H2(g)K3;
可得关系式③=①+②,因此K3=K1×K2;
故答案为:K3=K1×K2;
(3)①该反应在一定条件下的密闭容器中达到平衡后,为同时提高反应速率和二甲醚的产率,则速率加快而且平衡正移;
A.降低温度,反应速率减小,不符合题意,故a不选;
B.缩小容器体积,压强增大,速率加快,平衡正移二甲醚的产率提高,故b选;
C.加入催化剂,速率加快,但是平衡不移动,不符合题意,故c不选;
D.增加H2的浓度,速率加快,平衡正移二甲醚的产率提高,故d选;
E.分离出二甲醚,浓度减小,反应速率减小,不符合题意,故e不选;
故答案为:bd;
②CO(g)+H2O(g)=CO2(g)+H2(g)△H=-42 kJ?mol-1,由△H=反应物的键能总和-生成物的键能总和可得:
EC≡O+2×463kJ?mol-1-(2×802kJ?mol-1+436kJ?mol-1)=-42 kJ?mol-1,
解得:EC≡O=1072 kJ?mol-1,
故答案为:1072;
(4)①
| (1.00-0.50)mol/L |
| 2.00mol/L-c1 |
| 1 |
| 2 |
| (1.00-0.50)mol/L |
| t2min |
| 0.5 |
| t2 |
故答案为:1.00;
| 0.5 |
| t2 |
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ?mol-1,温度升高,化学反应速率加快,达到平衡的时间小于t2,平衡逆向移动,达到平衡时,CH3OCH3浓度小于1.00mol/L,CH3OCH3浓度随时问变化的关系图为
 ,故答案为:
,故答案为: .
.
点评:本题综合性较强,考查知识点全面,涉及熵变、化学平衡常数、反应热与键能的关系、化学反应速率计算、化学平衡影响因素等,较好的考查学生分析解决问题的能力,难度中等.

练习册系列答案
相关题目
对于排布在2s轨道上的电子,不能确定的是( )
| A、电子所在的电子层 |
| B、电子的自旋方向 |
| C、电子云的形状 |
| D、电子云的伸展方向 |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| B、常温下,pH≈5.5的0.1mol/LNaHC2O4溶液:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C、0.1mol/LNaHS溶液:c(OH-)+c(S2-)=c(H+)+c(H2S) |
| D、室温下,向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
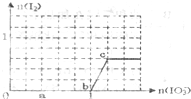 已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )
已知:还原性还原性HSO3->I-,氧化性IO3->I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如图所示.下列说法正确的是( )| A、反应过程中的氧化产物均为SO3 |
| B、a点时剩余NaHSO3的物质的量为1.2 mol |
| C、b点时的还原产物可能是KI或NaI |
| D、当溶液中I-与I2的物质的量之比为1:1时,加入的KIO3为1.1mol |
下列有关有机化合物的叙述正确的是( )
| A、进入人体的重金属盐能使蛋白质变性,所以会使人中毒 |
| B、卤代烃C4H8Cl2有四种同分异构体 |
| C、甲烷是天然气的主要成分,能发生加成反应 |
| D、用驴皮熬制成的胶(阿胶)是一种天然橡胶,属于天然高分子化合物 |
反应Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、升高温度该反应的正反应速率增大,逆反应速率减小 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |
下列说法正确的是( )
| A、4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA | ||||||||||
| B、一定温度下,氯化铵水解离子方程式:NH+4+H2O?NH3?H2O+H+,若用KW表示的离子积,Kb表示氨水电离常数,则氯化铵水解平衡常数K=KW/Kb | ||||||||||
| C、已知反应:2Fe3++2I-=2Fe2++I2:2Co(OH)3+2Cl-+6H+=2Co2++Cl2↑+6H2O:2Fe(OH)2+I2+2OH-=2Fe(OH)3+2I-;则在酸性溶液中氧化性:Fe3+>Co(OH)3>I2 | ||||||||||
D、已知
|
 元素X是地壳中含量最多的元素;元素Y基态原子的3p 轨道上有4个电子;元素Z 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.
元素X是地壳中含量最多的元素;元素Y基态原子的3p 轨道上有4个电子;元素Z 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.