题目内容
炽热的炉膛内有反应:C(s)+O2(g)=CO2(g)△H=-392kJ/mol,往炉膛内通入水蒸气时,有如下反应:C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ/mol,CO(g)+
O2(g)=CO2(g)△H=-282kJ,H2(g)+
O2(g)=H2O(g)△H=-241kJ/mol,由以上反应推断往炽热的炉膛内通入水蒸气时( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、不能节省燃料,但能使炉火瞬间更旺 |
| B、虽不能使炉火更旺,但可以节省燃料 |
| C、既能使炉火更旺,又能节省燃料 |
| D、既不能使炉火更旺,又不能节省燃料 |
考点:燃料的充分燃烧
专题:化学反应中的能量变化
分析:根据盖斯定律来分析煤的两种燃烧途径放出的热量,从而分析能否节省燃料和炉火是否瞬间更旺.
解答:
解:煤炭直接燃烧的热化学方程式:C(s)+O2(g)=CO2(g)△H=-392kJ/mol;
往炉膛内通入水蒸气时,有如下反应:C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ/mol ①,
CO(g)+
O2(g)=CO2(g)△H=-282kJ/mol②
H2(g)+
O2(g)=H2O(g)△H=-241kJ/mol③
由于碳先和水蒸气反应生成CO和氢气,气体在燃烧时比煤炭之间燃烧火焰更旺;
根据盖斯定律可知,将①+②+③可得:C(s)+O2(g)=CO2(g)△H=+131KJ/mol-282KJ/mol-241KJ/mol=-392kJ/mol,与煤炭直接燃烧的热效应是相同的,故并不节省燃料,故选A.
往炉膛内通入水蒸气时,有如下反应:C(s)+H2O(g)=CO(g)+H2(g)△H=+131kJ/mol ①,
CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
由于碳先和水蒸气反应生成CO和氢气,气体在燃烧时比煤炭之间燃烧火焰更旺;
根据盖斯定律可知,将①+②+③可得:C(s)+O2(g)=CO2(g)△H=+131KJ/mol-282KJ/mol-241KJ/mol=-392kJ/mol,与煤炭直接燃烧的热效应是相同的,故并不节省燃料,故选A.
点评:本题考查了燃料的燃烧和盖斯定律的运用,难度不大,注意知识的灵活运用.

练习册系列答案
相关题目
常温下,将足量CaCO3加入下列各体系中,溶解度最大的是( )
| A、10mL水 |
| B、10mL 0.1mol/LCaCl2溶液 |
| C、20mL 0.1mol/LNaHSO4 |
| D、40mL 0.1mol/LNa2CO3溶液 |
关于铜-锌-稀硫酸构成的原电池的有关叙述正确的是( )
| A、锌为负极,锌发生还原反应Zn-2e-=Zn2+ |
| B、电流方向经外电路由锌到铜 |
| C、工作时SO42-离子向正极移动 |
| D、外电路电子流入的一极为正极,电子流出的一极为负极 |
将NH4HCO3置于干的试管中加热,并使放出的气体依次通过盛有足量过氧化钠和足量碱石灰的干燥管,最后得到的气体有( )
| A、NH3 O2 |
| B、H2O O2 |
| C、CO2 O2 |
| D、O2 |
 铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成. 根据电化学知识回答下列问题.
根据电化学知识回答下列问题. 煤的液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术.
煤的液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术.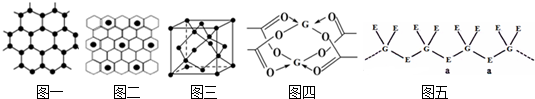
 ”表示),原子分布如图二所示,该物质的化学式为
”表示),原子分布如图二所示,该物质的化学式为