题目内容
20.下列有关化学用语表示正确的是( )| A. | 质量数为31的磷原子:3115P | B. | 氟原子的结构示意图: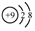 | ||
| C. | CaCl2的电子式: | D. | 明矾的化学式:Al2(SO4)3 |
分析 A.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
B.氟原子的核电荷数=核外电子总数=9,最外层含有7个电子;
C.两个氯离子不能合并;
D.明矾为十二水合硫酸铝钾.
解答 解:A.质量数为31的磷原子的质量数=15+16=31,该原子正确的表示方法为:3115P,故A正确;
B.氟原子的核电荷数、核外电子总数都是9,其正确的结构示意图为: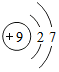 ,故B错误;
,故B错误;
C.氯化钙为离子化合物,电子式中需要标出阴阳离子所带电荷,氯化钙正确的电子式为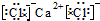 ,故C错误;
,故C错误;
D.明矾化学式中含有结晶水,其正确的化学式为:KAl(SO4)2•12H2O,故D错误;
故选A.
点评 本题考查常见化学用语的表示方法,题目难度不大,涉及电子式、原子结构示意图、元素符号、化学式等知识,注意掌握常见化学用语的书写原则,试题培养学生的规范答题能力.

练习册系列答案
相关题目
17.实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是( )
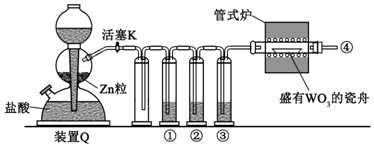

| A. | ①、②、③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液 | |
| B. | 管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体浓度 | |
| C. | 结束反应时,先关闭活塞K,再停止加热 | |
| D. | 装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 |
15.某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下.
向硝酸酸化的0.05mol•L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色.
(1)检验产物
①取少量黑色固体,洗涤后,加入足量加入足量稀盐酸(或稀硫酸)酸化,固体未完全溶解(填操作和现象),证明黑色固体中含有Ag.
②取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有Fe2+.
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是Fe+2Fe3+=3Fe2+(用离子方程式表示).针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测.同时发现有白色沉淀产生,且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
(资料:Ag+与SCN-生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据白色沉淀现象,判断溶液中存在Ag+,可产生Fe3+.
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因.实验Ⅱ可证实假设d成立.
实验Ⅰ:向硝酸酸化的NaNO3溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后溶液几乎无色.
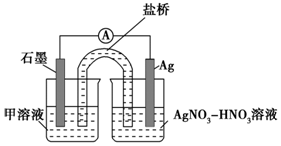
实验Ⅱ:装置如图.其中甲溶液是FeCl2/FeCl3,操作及现象是按图连接好装置,电流表指针发生偏转.
(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因:i→ii Ag++Fe2+=Ag+Fe3+,反应生成Fe3+的使Fe3+增加,红色变深,ii→iii 空气中氧气氧化SCN-,红色变浅.
向硝酸酸化的0.05mol•L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色.
(1)检验产物
①取少量黑色固体,洗涤后,加入足量加入足量稀盐酸(或稀硫酸)酸化,固体未完全溶解(填操作和现象),证明黑色固体中含有Ag.
②取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有Fe2+.
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是Fe+2Fe3+=3Fe2+(用离子方程式表示).针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测.同时发现有白色沉淀产生,且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
| 序号 | 取样时间/min | 现象 |
| ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
| ⅱ | 30 | 产生白色沉淀;较3min时量少;溶液红色较3min时加深 |
| ⅲ | 120 | 产生白色沉淀;较30min时量少;溶液红色较3 0min时变浅 |
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据白色沉淀现象,判断溶液中存在Ag+,可产生Fe3+.
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因.实验Ⅱ可证实假设d成立.
实验Ⅰ:向硝酸酸化的NaNO3溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后溶液几乎无色.
实验Ⅱ:装置如图.其中甲溶液是FeCl2/FeCl3,操作及现象是按图连接好装置,电流表指针发生偏转.

(3)根据实验现象,结合方程式推测实验ⅰ~ⅲ中Fe3+浓度变化的原因:i→ii Ag++Fe2+=Ag+Fe3+,反应生成Fe3+的使Fe3+增加,红色变深,ii→iii 空气中氧气氧化SCN-,红色变浅.
5.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 无色透明的溶液中:Fe3+、Mg2+、SCN -、Cl - | |
| B. | c(H+)/c(OH-)=1×10 -12的溶液中:K+、Na+、CO32-、NO3- | |
| C. | c(Fe2+ )=1 mol•L-1的溶液中:K+、NH4+、MnO4-、SO42- | |
| D. | 能使甲基橙变红的溶液中:Na+、NH4+、SO42-、HCO3- |
3.下列说法正确的是( )
| A. | 1 mol葡萄糖能水解生成2molCH3CH2OH和2molCO2 | |
| B. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| C. | 油脂不是高分子化合物,1mol油脂完全水解生成1mol甘油和3 mol高级脂肪酸(盐) | |
| D. | 乙烯能使酸性高锰酸钾溶液和溴水褪色,二者反应原理相同 |
20.下列实验操作所得的现象及结论均正确的是( )
| 选项 | 实验操作 | 现象及结论 |
| A | 将AlC13溶液加热蒸干 | 得到白色固体,成分为纯净的AlC13 |
| B | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,则Na2SO3己变质 |
| C | 用量筒量取一定体积的浓硫酸时,仰视读数 | 所量取的浓硫酸体积偏大 |
| D | 向FeI2溶液中通入少量C12 | 溶液变黄,则C12的氧化性强于Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
6.短周期主族元素A、B、C、D、E的原子序数依次增大,考古时利用A元素的某种同位素可以测定一些文物的年代,A原子的最外层比B原子的最外层少2个电子,A、B、C三种元素能组成离子化合物C2AB3,B、D同主族.下列说法正确的是( )
| A. | 含氧酸的酸性由强到弱的顺序:E、D、A | |
| B. | 简单气态氢化物的稳定性由强到弱的顺序:B、D、E | |
| C. | B、C、E形成的共价化合物CEB可以用来杀菌消毒 | |
| D. | 简单离子半径由大到小的顺序:D、E、B、C |
 .
.
 .
.