题目内容
5. 利用所学化学知识解答问题:
利用所学化学知识解答问题:(1)基态Cu2+的核外电子排布式为1s22s22p63s23p63d9,在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因:结构上Cu2+为3d9,而Cu+为3d10全充满更稳定.根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于ds区.
(2)下列叙述不正确的是ac.(填字母)
a.HCHO和CO2分子中的中心原子均采用sp杂化
b.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水
c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子
d.CO2晶体的熔点、沸点都比二氧化硅晶体的低,原因是CO2为分子晶体而二氧化硅是原子晶体
(3)氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式N≡C-O-H.其中的C的杂化类型为sp杂化,写出一种与 CN-互为等电子体的单质分子式N2.
(4)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是具有孤对电子.
②六氰合亚铁离子[Fe(CN)6]4-中不存在b.
a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
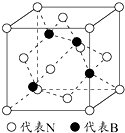
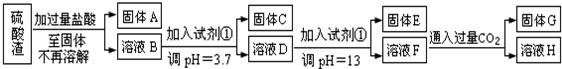
(5)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有4个氮原子,4个硼原子,设氮原子半径为a pm,硼的原子半径b pm,求该晶胞的空间利用率$\frac{{\sqrt{3}π({{a^3}+{b^3}})}}{{4{{({a+b})}^3}}}$×100%.(用含a、b的代数式表示)
分析 (1)Cu元素原子核外电子数为29,其基态原子的电子排布式为1s22s22p63s23p43d104s1,Cu原子失去4s、3d能级的1个电子形成Cu2+;根据构造原理书写Cu+基态核外电子排布式,轨道处于全空、半满或全满时最稳定;根据Cu的外围电子排布式分析;
(2)A、HCHO中的中心原子为sp2杂化;
B、甲醛中含有羟基,与水可以形成氢键;
C、苯中碳碳键含有6个σ键,每个碳氢键含有一个σ键,苯分子中一共含有12个,故C错误;
D、分子晶体晶体的熔点、沸点比原子晶体低;
(3)碳为四价,氮为三价,氧为两价,氰酸(HOCN)是一种链状分子,且其分子内各原子最外层均已达到稳定结构,故N≡C-O-H;氰酸中C原子形成2个σ键、没有孤电子对;CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质;
(4)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键;
(5)根据均摊法计算晶胞中B、N原子数目,进而计算晶胞中含有B、N原子总体积,计算晶胞的体积,晶胞的空间利用率=$\frac{晶胞中B、Ni原子总体积}{晶胞体积}$×100%.
解答 解:(1)Cu元素原子核外电子数为29,其基态原子的电子排布式为1s22s22p63s23p63d104s1,Cu原子失去4s、3d能级的1个电子形成Cu2+,Cu2+的核外电子排布式为:1s22s22p63s23p63d9;Cu+基态核外电子排布式1s22s22p63s23p63d10或[Ar]3d10 ,原子轨道处于全空、半满或全满时最稳定,结构上Cu2+为3d9,而Cu+为3d10全充满更稳定;Cu的外围电子排布式为3d104s1,Cu属于第IB族元素,在周期表中位于ds区;
故答案为:1s22s22p63s23p63d9;结构上Cu2+为3d9,而Cu+为3d10全充满更稳定;ds;
(2)a.HCHO中的中心原子为sp2杂化,故a错误;
b.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水,故b正确;
c.苯中碳碳键含有6个σ键,每个碳氢键含有一个σ键,苯分子中一共含有12个σ键,故c错误;
d.CO2为分子晶体,二氧化硅是原子晶体,所以CO2晶体的熔点、沸点都比二氧化硅晶体的低,故d正确;
故答案为:ac;
(3)碳为四价,氮为三价,氧为两价,氰酸(HOCN)是一种链状分子,且其分子内各原子最外层均已达到稳定结构,故N≡C-O-H;氰酸中C原子形成2个σ键、没有孤电子对,C的杂化类型为sp杂化;CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质为N2,
故答案为:N≡C-O-H;sp杂化;N2;
(4)①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;
故答案为:具有孤对电子;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键,所以CN-中共价键、配位键、σ键、π键;
故答案为:b;
(5)方氮化硼晶胞结构与金刚石类似,晶胞结构图为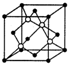 ,B占据立方体的8个顶点和6个面心,所以B原子数目为=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,N原子数目=4;B原子半径为bpm,则晶胞中B原子总体积=4×$\frac{4}{3}$×π×(b)3pm3=$\frac{16}{3}$πb3pm3,N原子半径为a pm,则晶胞中N原子总体积=4×$\frac{4}{3}$×π×(a)3pm3=$\frac{16}{3}$πa3cm3,故晶胞中B、N原子总体积=$\frac{16}{3}$π(a3+b3)pm3,根据硬球接触模型可知,体对角线四分之一处的原子与顶点上的原子紧贴,设晶胞边长为x,所以$\frac{1}{4}$×($\sqrt{3}$x)=a+b,x=$\frac{4}{\sqrt{3}}$(a+b),晶胞体积=x3=$\frac{64}{3\sqrt{3}}$(a+b)3pm3,所以间利用率=$\frac{\frac{16}{3}π({a}^{3}+{b}^{3})p{m}^{3}}{\frac{64}{3\sqrt{3}}(a+b)^{3}pm{\;}^{3}}$×100%=$\frac{\sqrt{3}π({a}^{3}+{b}^{3)}}{4(a+b){\;}^{3}}$×100%;
,B占据立方体的8个顶点和6个面心,所以B原子数目为=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,N原子数目=4;B原子半径为bpm,则晶胞中B原子总体积=4×$\frac{4}{3}$×π×(b)3pm3=$\frac{16}{3}$πb3pm3,N原子半径为a pm,则晶胞中N原子总体积=4×$\frac{4}{3}$×π×(a)3pm3=$\frac{16}{3}$πa3cm3,故晶胞中B、N原子总体积=$\frac{16}{3}$π(a3+b3)pm3,根据硬球接触模型可知,体对角线四分之一处的原子与顶点上的原子紧贴,设晶胞边长为x,所以$\frac{1}{4}$×($\sqrt{3}$x)=a+b,x=$\frac{4}{\sqrt{3}}$(a+b),晶胞体积=x3=$\frac{64}{3\sqrt{3}}$(a+b)3pm3,所以间利用率=$\frac{\frac{16}{3}π({a}^{3}+{b}^{3})p{m}^{3}}{\frac{64}{3\sqrt{3}}(a+b)^{3}pm{\;}^{3}}$×100%=$\frac{\sqrt{3}π({a}^{3}+{b}^{3)}}{4(a+b){\;}^{3}}$×100%;
故答案为:4;4;$\frac{{\sqrt{3}π({{a^3}+{b^3}})}}{{4{{({a+b})}^3}}}$×100%.
点评 本题是对物质结构知识的综合考查,涉及核外电子排布规律、分子结构与性质、杂化轨道、晶胞计算、空间利用率的计算等,需要学生具有一定的空间想象与数学计算能力,题目难度中等.

| A. | Na+、Ag+、NO3-、Cl- | B. | K+、Ba2+、Cl-、CO32- | ||
| C. | Na+、Fe3+、NO3-、SO42- | D. | Na+、Mg2+、OH-、NO3- |
| A. | 在精炼铜或电镀铜的过程中,当阳极析出铜64g转移电子数均为2NA | |
| B. | 24g石墨烯(单层石墨)中含有六元环的个数为NA | |
| C. | 1.0mo1•L-1的Na2CO3溶液中所含阴离子数大于NA个 | |
| D. | 1mol的甲基(-CH3)中所含的电子数为10NA |
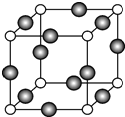 已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期元素且最外层只有2对成对电子,F元素与Cr元素位于同一周期的副族元素中且基态原子的最外层电子数与Cr原子相同.
已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素.E是第四周期元素且最外层只有2对成对电子,F元素与Cr元素位于同一周期的副族元素中且基态原子的最外层电子数与Cr原子相同. .
.