题目内容
18.CO2的摩尔质量是44g/mol;2molCO2的质量是88g;在标准状况下所占的体积约为44.8L;所含的分子数目约为1.204×1024个;所含氧原子的数目约为2.408×1024个.分析 结合m=nM、V=nVm、N=nNA及分子构成计算.
解答 解:CO2的摩尔质量是44g/mol;2molCO2的质量是2mol×44g/mol=88g;在标准状况下所占的体积约为2mol×22.4L/mol=44.8L;所含的分子数目约为2×6.02×1023=1.204×1024个;所含氧原子的数目约为2×2×6.02×1023=2.408×1024个,
故答案为:44g/mol;88g;44.8L;1.204×1024个;2.408×1024个.
点评 本题考查物质的量的计算,为高频考点,把握以物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
9.某海域海水一些化学成分如表所示,已知:25℃时,
Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11.
某化学小组同学欲在实验制备MgCl2,并提取Zn.设计流程如图:
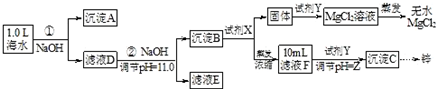
[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH> 7.0(填“>”、“<”、“﹦”),其原因是HCO3-+H2O?H2CO3+OH-(写离子方程式).
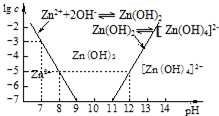
(2)如图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图.请结合图中数据回答:试剂Y的化学式为HCl;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH范围为8<pH<12.
(3)同学们发现,把MgCl2溶液蒸干、灼烧所得的白色固体难溶于水,你认为其主要成分是MgO.原因是(用化学方程式表示)MgCl2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2HCl↑、Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp=10-17.
Ksp(CaCO3)=2.8×10-9,Ksp(MgCO3)=6.8×10-6,Ksp[Mg(OH)2]=1.8×10-11.
| 海水成分 | Na+ | Ca2+ | Mg2+ | HCO3- | Zn2+ |
| 含量/mol•L-1 | 0.4 | 0.002 | 0.045 | 0.002 | 10-7 |

[假设①②过程溶液体积不变,忽略分离过程的损失]
(1)25℃时测得海水的pH> 7.0(填“>”、“<”、“﹦”),其原因是HCO3-+H2O?H2CO3+OH-(写离子方程式).
(2)如图为溶液pH与对应的Zn2+、[Zn(OH)4]2-物质的量浓度的对数坐标图.请结合图中数据回答:试剂Y的化学式为HCl;由滤液F到沉淀C过程(一般认为离子浓度低于10-5mol/L就是沉淀完全),则调节的pH范围为8<pH<12.

(3)同学们发现,把MgCl2溶液蒸干、灼烧所得的白色固体难溶于水,你认为其主要成分是MgO.原因是(用化学方程式表示)MgCl2+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2HCl↑、Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O.
(4)由图中c(Zn2+)计算Zn(OH)2的溶度积Ksp=10-17.
6.下列说法正确的是( )
| 化学式 | 电离常数 |
| CH3COOH | Ka=1.76×10-5 |
| H2SO3 | Ka1=1.54×10-2 |
| Ka2=1.02×10-7 | |
| HF | Ka=6.03×10-4 |
| A. | 在1mol•L-1NaHA(酸式盐)溶液中一定存在:c(Na+)=c(H2A)+c(HA-)+c(A2-) | |
| B. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | 已知某温度下常见弱酸的电离平衡常数如上表:相同物质的量浓度的CH3COONa、NaF、Na2SO3、NaHSO3水溶液,溶液中离子总数由小到大排列的顺序是Na2SO3<CH3COONa<NaF<NaHSO3 | |
| D. | pH均等于3的醋酸与盐酸溶液等体积混合后,溶液的pH基本不变 |
13.某学生进行了“浓度影响化学反应速率”的探究实验,原始数据记录如下:
(1)比较三组数据,初步得出的结论是:当其他条件不变时,H2SO4(填化学式)的浓度增加,反应速率加快(填“加快”、“减慢”或“不变”);
(2)写出该反应的化学方程式Zn+H2SO4=ZnSO4+H2↑,该反应中还原剂是Zn,从反应分类角度来看,该反应既属于氧化还原反应,又属于置换反应(填四大基本反应类型之一).
| Zn的质量 | H2SO4的浓度 | 收集20mL H2所需的时间 | |
| ① | 12g(锌粒) | 0.1mol/L | 153s |
| ② | 10g(锌粉) | 0.1mol/L | 125s |
| ③ | 10g(锌粉) | 0.2mol/L | 62s |
(2)写出该反应的化学方程式Zn+H2SO4=ZnSO4+H2↑,该反应中还原剂是Zn,从反应分类角度来看,该反应既属于氧化还原反应,又属于置换反应(填四大基本反应类型之一).
3.已知:Ka为平衡常数,pKa=-lgKa,25℃时,H2A的 pKa1=1.85,pKa2=7.19,用 0.1mol•L-1NaOH溶液滴定20mL0.1mol•L-1H2A溶液的滴定曲线如图所示(曲线上的数字为 pH).下列说法不正确的是( )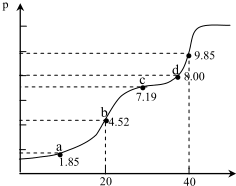

| A. | a 点所得溶液中;2n(H2A)+n(A2-)=0.002mol | |
| B. | b 点所得溶液中:c(H2A)+c(H+)=c(A2-)+c(OH-) | |
| C. | c 点所得溶液中:c(Na+)<3c(HA-) | |
| D. | d 点所得溶液中:c(Na+)>c(A2-)>c(HA-) |
18.下列说法正确的是( )
| A. | 随原子序数递增,ⅦA族元素的最高价氧化物对应水化物酸性逐渐增强 | |
| B. | 第三周期元素中(除稀有气体元素)简单离子半径最小的元素,其氧化物具有两性 | |
| C. | 第三周期气态氢化物的沸点均为同主族中沸点最低 | |
| D. | 第二周期元素(除稀有气体元素)的最高化合价数值逐渐增大 |

 ;
; ,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.
,⑥所需的无机试剂及反应条件是氢氧化钠醇溶液、加热.