题目内容
7.分子式为C5H10O3的有机物,在一定条件下能发生如下反应:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;
②在一定温度及浓硫酸存在下,能生成一种使溴水褪色的物质;
③在一定温度及浓硫酸存在下,能生成一种分式为C5H8O2的五元环状化合物.
则C5H10O3的结构简式为 ( )
| A. | HOCH2CH2COOCH2CH3 | B. | HOCH2CH2CH2CH2COOH | ||
| C. | CH3CH2CH(OH)CH2COOH | D. | CH3CH(OH)CH2CH2COOH |
分析 ①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有-COOH、-OH;
②脱水生成一种能使溴水褪色的物质,则-OH邻位上的C原子上有H原子;
③在浓硫酸存在下,还能生成一种分子式为C5H8O2的五元环状化合物,可知-COOH和-OH之间有3个碳原子.
解答 解:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应,说明分子中含有-COOH、-OH;
②脱水生成一种能使溴水褪色的物质,则-OH邻位上的C原子上有H原子;
③在浓硫酸存在下,还能生成一种分子式为C5H8O2的五元环状化合物,可知-COOH和-OH之间有3个碳原子,
结合有机物的分子式C5H10O3,可知其结构简式为CH3CH(OH)CH2CH2COOH等,
故选D.
点评 本题考查有机物的推断,题目难度不大,根据题目信息确定含有的官能团及位置为解答该题的关键,可用排除法进行解答.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
18.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、Na+、ClO、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Mg2+、NH4+、Cl-、SO42- |
18.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 达到化学平衡时,v正=v逆=0 | |
| B. | 化学反应速率关系是2v(NH3)=3v(H2O) | |
| C. | 达到化学平衡时,O2的浓度不再改变 | |
| D. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
15.常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液.下列说法正确的是( )
| A. | ④和②混合溶液中:c(H+)=c(OH-) | |
| B. | ①与④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | ②和③混合溶液中:c(H+)>c(OH-) | |
| D. | 四种溶液稀释100倍,溶液pH:③>④>②>① |
2.天然纤维的吸湿性优于合成纤维,合成纤维中吸湿性较好的是( )
| A. | 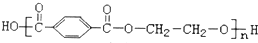 涤纶 涤纶 | B. | 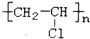 氯纶 氯纶 | ||
| C. | 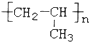 丙纶 丙纶 | D. | 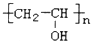 维纶 维纶 |
12.在100℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下:[2NO2(g)?N2O4(g)△H<0],下列说法正确的是( )
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A. | 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2) | |
| B. | 平衡时,升高温度,Ⅰ中速率减慢,Ⅱ中速率加快 | |
| C. | 当密度不变时,上述反应即达平衡 | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
19.“地球一小时”熄灯活动,以倡导节能减排理念.下列不能达到节能减排目的是( )
| A. | 利用太阳能发电 | B. | 用家用汽车代替公交车 | ||
| C. | 利用化石燃料制造燃料电池 | D. | 用节能灯代替白炽灯 |
17.下列物质中,不属于合金的是( )
| A. | 碳素钢 | B. | 水银 | C. | 青铜 | D. | 黄铜 |
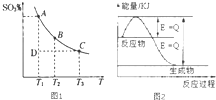 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.