题目内容
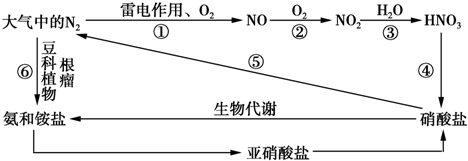
下表是元素周期表的一部分,针对表中的①-⑩元素按要求回答下列问题:
(1)在①-⑩元素中,化学性质最不活泼的元素是 (填元素符号),化学性质最活泼的金属元素是 (填元素符号).
(2)在最高价氧化物对应水化物中,酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 .
(3)最高价氧化物属于两性氧化物的元素是 (填元素符号),写出该元素的最高价氧化物与NaOH溶液反应的离子方程式
(4)比较元素的气态氢化物的稳定性:② ③;最高价氧化物对应水化物的酸性强弱:② ⑥.
(5)⑥的最高价氧化物与烧碱溶液反应的化学方程式为
(6)④元素与⑧元素形成的化合物的化学式是 ,高温灼烧该化合物时,火焰呈 色.
| ⅠA | ⅡA | ⅢA | IⅤA | ⅤA | ⅤⅠA | ⅤⅡA | 0族 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物对应水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物属于两性氧化物的元素是
(4)比较元素的气态氢化物的稳定性:②
(5)⑥的最高价氧化物与烧碱溶液反应的化学方程式为
(6)④元素与⑧元素形成的化合物的化学式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知①为C、②为N、③为O、④为Na、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar、⑩为K.
(1)稀有气体的化学性质最不活泼;同周期自左而右金属性减弱、同主族自上而下金属性增强;
(2)元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,元素金属性越强,对应的最高价氧化物对应水化物的碱性越强;
(3)氧化铝是两性氧化物,氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水;
(4)非金属性越强,氢化物越稳定,最高价含氧酸的酸性越强;
(5)⑥的最高价氧化物为SiO2,与烧碱溶液反应生成硅酸钠与水;
(6)④元素与⑧元素形成的化合物为NaCl,钠元素焰色反应为黄色.
(1)稀有气体的化学性质最不活泼;同周期自左而右金属性减弱、同主族自上而下金属性增强;
(2)元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,元素金属性越强,对应的最高价氧化物对应水化物的碱性越强;
(3)氧化铝是两性氧化物,氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水;
(4)非金属性越强,氢化物越稳定,最高价含氧酸的酸性越强;
(5)⑥的最高价氧化物为SiO2,与烧碱溶液反应生成硅酸钠与水;
(6)④元素与⑧元素形成的化合物为NaCl,钠元素焰色反应为黄色.
解答:
解:由元素在周期表中位置,可知①为C、②为N、③为O、④为Na、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar、⑩为K.
(1)稀有气体Ar的化学性质最不活泼;同周期自左而右金属性减弱、同主族自上而下金属性增强,上述元素中K的金属性最强,其性质最活泼,故答案为:Ar;K;
(2)上述元素中Cl非金属性最强,故最高价氧化物对应水化物的酸性最强的酸是HClO4,K的金属性最强,故最高价氧化物对应水化物的碱性最强的是KOH,故答案为:HClO4;KOH;
(3)氧化铝是两性氧化物,氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:Al;Al2O3+2OH-=2AlO2-+H2O;
(4)非金属N<O,故氢化物稳定性NH3<H2O,非金属性N>Si,故最高价含氧酸的酸性:硝酸>硅酸,故答案为:<;>;
(5)⑥的最高价氧化物为SiO2,与烧碱溶液反应生成硅酸钠与水,反应方程式为:SiO2+2NaOH=Na2SiO3+H2O,故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(6)④元素与⑧元素形成的化合物为NaCl,高温灼烧该化合物时,火焰呈黄色,故答案为:NaCl;黄色.
(1)稀有气体Ar的化学性质最不活泼;同周期自左而右金属性减弱、同主族自上而下金属性增强,上述元素中K的金属性最强,其性质最活泼,故答案为:Ar;K;
(2)上述元素中Cl非金属性最强,故最高价氧化物对应水化物的酸性最强的酸是HClO4,K的金属性最强,故最高价氧化物对应水化物的碱性最强的是KOH,故答案为:HClO4;KOH;
(3)氧化铝是两性氧化物,氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:Al;Al2O3+2OH-=2AlO2-+H2O;
(4)非金属N<O,故氢化物稳定性NH3<H2O,非金属性N>Si,故最高价含氧酸的酸性:硝酸>硅酸,故答案为:<;>;
(5)⑥的最高价氧化物为SiO2,与烧碱溶液反应生成硅酸钠与水,反应方程式为:SiO2+2NaOH=Na2SiO3+H2O,故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(6)④元素与⑧元素形成的化合物为NaCl,高温灼烧该化合物时,火焰呈黄色,故答案为:NaCl;黄色.
点评:本题考查元素周期表与元素周期律的综合应用,难度不大,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
下列反应的离子方程式正确的是( )
A、乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH-
| ||
B、向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-
| ||
| C、苯酚钠溶液中通入少量二氧化碳:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | ||
D、乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH-
|
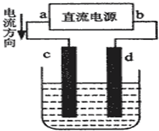 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )| A、a为负极、b为正极 |
| B、电解过程中,c电极发生还原反应 |
| C、电解过程中,d电极质量增加 |
| D、电解过程中,氯离子浓度不变 |
 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、常压下五种元素的单质中,Z单质的熔点最高 |
| B、Z2水溶液中通入YO2后褪色,表现了YO2的漂白性 |
| C、工业上合成X的氢化物采用高温高压催化剂条件 |
| D、Y、Z的阴离子电子层结构都与R原子的相同 |
两种金属混合粉末12克,与足量盐酸反应时生成标准状况下11.2L氢气,符合上述情况的金属混合物是( )
| A、Mg和Fe |
| B、Fe和Zn |
| C、Mg和Al |
| D、Al和Fe |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、标准状况下,11.2L H2O 中所含的分子数为0.5NA |
| B、常温下,32g O3中所含的原子数为2NA |
| C、1.0 mol?L-1NaOH溶液中所含Na+离子数为NA |
| D、5.6g Fe与2.24L Cl2充分反应,转移的电子数为0.2 NA |