��Ŀ����
�� ��1����֪��N2��g��+O2��g��=2NO��g��; ��H=+180��5 kJ��mol-1
�� �� 4NH3��g��+5O2��g��=4NO��g��+6H2O��g������H=-905 kJ��mol-1
2H2��g��ʮO2��g��=2H2O��g������H=--483��6 kJ��mol-1
��N2��g��+3H2��g����![]() ��2NH3��g���ġ�H=���������� ��
��2NH3��g���ġ�H=���������� ��
�� ��2����һ�������£���2mol N2��5mol H2�����һ��10 L���ܱ������У���Ӧ�����ͼ1��ʾ��
����5min�ڵ�ƽ����Ӧ����v��NH3���������������� ��
�ڴﵽƽ��ʱNH3���������Ϊ���������������������� ��

�������������������������� ͼ1�������������������� ͼ2 ��ⷨ�ϳɰ�װ��
�� ��3����������ѧ�Ҳ��ø����ӵ����Ե�SCY�մɣ��ܴ���H+��Ϊ���ʣ�������������������ϵĽ����ٶ�Ʒ��Ĥ���缫��ʵ���˸�ת���ʵĵ�ⷨ�ϳɰ���װ����ͼ2�����ٵ缫A�Ϸ����ĵ缫��Ӧʽ�������������������� ����
��1��-92��4kJ��mol-1
��2����0.04mol��L-1��min-1 ��40%
��3��N2+6e-+6H+=2NH3

 С�����ϵ�д�
С�����ϵ�д���11�֣��������ϰ�װ��Ч��ת��������ʹ����β���е���Ҫ��Ⱦ�CO��NOx��̼�⻯����������Ӧ�����������ʣ���������β����Ⱦ��
��1����֪��N2(g)+ O2(g)="2NO(g)" ��H="+180.5" kJ��mol��1
2C(s)+ O2(g)="2CO(g) " ��H=��221.0 kJ��mol��1
C(s)+ O2(g)=CO2(g) ��H=��393.5 kJ��mol��1
��β��ת���ķ�Ӧ֮һ��2NO(g)+2CO(g)=N2(g)+2CO2(g) ��H�� ��
����֪��N2��O2�����л�ѧ���ļ��ֱܷ���946 kJ��mol��1��497 kJ��mol��1����NO�����л�ѧ���ļ���Ϊ ���������� kJ��mol��1��
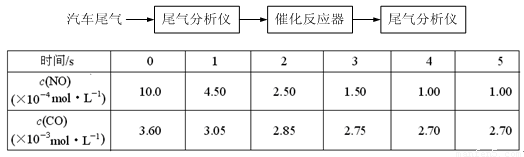
��2��ij�о���ѧϰС���ڼ�����Ա��ָ���£���ij�¶�ʱ������������̽��ij�ִ��������µķ�Ӧ���ʣ������崫������ò�ͬʱ���NO��COŨ�������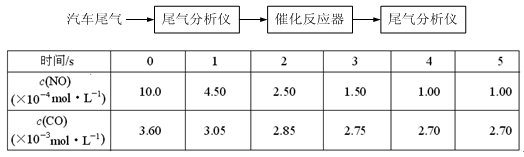
��ش���������(���������¶ȱ仯�Դ�����Ч�ʵ�Ӱ��)��
��ǰ3s�ڵ�ƽ����Ӧ����v (N2) = _________________________��
���ڸ��¶��£���Ӧ��ƽ�ⳣ��K = ������ ����ֻд����������
�۸ÿ��淴Ӧ��S 0���>������<������������_______________������¡��������¡����κ��¶ȡ��������Է����С�
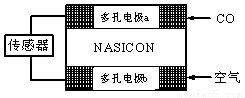
��3��CO��������ȼ�ϵ��Ϊ����ԭ������װ����ͼ��ʾ���õ���е����Ϊ�����ƣ������ƣ�����O2-�����ڹ������NASICON�������ƶ�������˵��������� 
| A�������ĵ缫��ӦʽΪ�� CO+O2���D2e-��CO2 |
| B������ʱ�缫b��������O2-�ɵ缫a����缫b |
| C������ʱ�����ɵ缫aͨ������������缫b |
| D����������ͨ���ĵ���Խ��β����CO�ĺ���Խ�� |

 CaS
+4CO��
CaS
+4CO��