题目内容
在4L密闭容器中充入6molA气体和5molB气体,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol/L,下列判断正确的是 ( )
2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol/L,下列判断正确的是 ( )
A.x=1
B.B的转化率为20%
C.平衡时A的浓度为1.50mol/L
D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
B
【解析】
试题分析:【解析】
达到平衡时,生成了2molC,D的物质的量为4L×0.5mol/L=2mol,
3A(g)+B(g)?2C(g)+xD(g)
起始:6mol 5mol 0 0
转化:3mol 1mol 2mol xmol
平衡:3mol 4mol 2mol 2mol
由以上分析可知x=2,A错误;B的转化率为1/5×100%=20%,B正确;平衡时A的浓度为3/4=0.75mol/L, C错误;反应前后气体的物质的量不变,则压强不变,D错误。
考点:考查考查化学平衡的计算

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
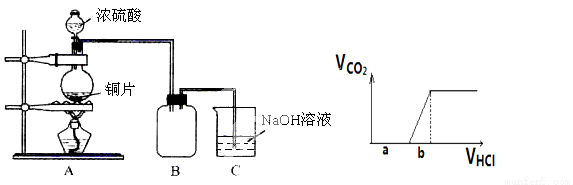

 CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是 2C(g)(正反应吸热),下列图象中正确的是 ( )
2C(g)(正反应吸热),下列图象中正确的是 ( )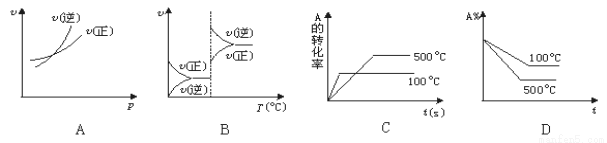
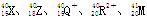 ,所属元素的种类是5种
,所属元素的种类是5种