题目内容
根据下列热化学方程式:
①C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
②H2(g)+1/2O2(g)=H2O(l) ΔH2=-285.8 kJ/mol
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3 kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
A.ΔH=+244.1kJ/mol B.ΔH=-488.3kJ/mol
C.ΔH=-996.6kJ/molD.ΔH=+996.6kJ/mol
B
【解析】
试题分析:(①+②)×2-③,整理可得:2C(s)+2H2(g)+O2(g)=CH3COOH(l) ΔH=(ΔH1+ΔH2)×2-ΔH3=-488.3kJ/mol,因此选项是B。
考点:考查盖斯定律的应用及反应热的计算的知识。

练习册系列答案
相关题目
 2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1 mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示:
mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示: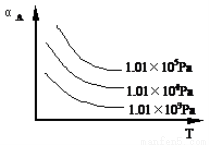
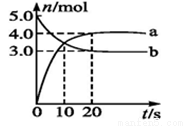
 4NO2(g)+O2(g) ΔH>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是 ( )
4NO2(g)+O2(g) ΔH>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中正确的是 ( )