题目内容
下列化学用语正确的是( )
A、氯化氢的电子式H+[:
| ||||
B、镁的原子结构示意图 | ||||
| C、次氯酸的结构式 H-Cl-O | ||||
| D、实验室制取氯气的离子方程式MnO2+4HCl(浓)=Cl2+Mn2++2H2O |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图,离子方程式的书写
专题:
分析:A.氯化氢为共价化合物,分子中不存在阴阳离子;
B.镁原子的核电荷数=核外电子总数=12;
C.次氯酸的中心原子为O原子,分子中不存在氢氯键;
D.浓盐酸在离子方程式中需要拆开,且该反应需要加热.
B.镁原子的核电荷数=核外电子总数=12;
C.次氯酸的中心原子为O原子,分子中不存在氢氯键;
D.浓盐酸在离子方程式中需要拆开,且该反应需要加热.
解答:
解:A.氯化氢为共价化合物,氯原子最外层达到8电子稳定结构,氯化氢正确的电子式为: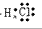 ,故A错误;
,故A错误;
B.镁原子的核电荷数、核外电子总数都是12,最外层为2个电子,其原子结构示意图为: ,故B正确;
,故B正确;
C.次氯酸分子中存在1个氢氧键和1个氧氯键,次氯酸正确的结构式为:H-O-Cl,故C错误;
D.向MnO2固体中加入浓盐酸并加热,发生反应生成氯气,浓盐酸中的氯化氢需要拆开,正确的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故D错误;
故选B.
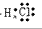 ,故A错误;
,故A错误;B.镁原子的核电荷数、核外电子总数都是12,最外层为2个电子,其原子结构示意图为:
 ,故B正确;
,故B正确;C.次氯酸分子中存在1个氢氧键和1个氧氯键,次氯酸正确的结构式为:H-O-Cl,故C错误;
D.向MnO2固体中加入浓盐酸并加热,发生反应生成氯气,浓盐酸中的氯化氢需要拆开,正确的离子方程式为:MnO2+4H++2Cl-
| ||
故选B.
点评:本题考查了离子方程式、电子式、原子结构示意图、结构式等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确原子结构示意图与离子结构示意图、离子化合物与共价化合物的电子式的区别.

练习册系列答案
相关题目
室温下,某溶液中由水电离产生的c(H+)等于10-10 mol/L,该溶液的溶质不可能是( )
| A、NaHSO4 |
| B、NaCl |
| C、HCl |
| D、Ba(OH)2 |
三种难溶金属硫化物的溶度积常数(25℃):
下列有关说法中正确的是( )
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
| A、25℃时,CuS的溶解度大于MnS的溶解度 |
| B、25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol?L-1 |
| C、因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生 |
| D、除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
元素A和B的原子序数都小于18.已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-2b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有( )
| A、能与水反应 |
| B、能与氢氧化钠溶液反应 |
| C、能与硫酸反应 |
| D、能与碳酸钠溶液反应 |
下列叙述正确的是( )
| A、同温同压下,相同体积的物质,它们的物质的量必相同 |
| B、常温常压下,等质量的N2与CO所含分子数相同 |
| C、V L O2的质量一定比V L CO2的质量小 |
| D、A容器中的H2与B容器中的NH3所含原子总数相等,由两容器的体积比为2:1 |
 ,试回答:
,试回答: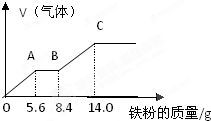 某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)
某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)