题目内容
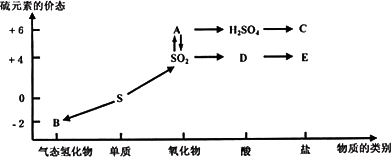
人们认识和应用物质常从两方面入手,一是从物质的类别认识该物质可能跟哪些物 质发生反应;二是从物质所含元素的化合价分析该物质是否具有氧化性或还原性.下图是 硫元素的各个价态与物质类别的对应关系: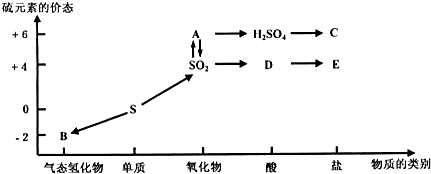
(1)写出指定物质的化学式:A
(2)D转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式
(3)若C是铜盐,试写出由H2SO4---C的化学方程式
(4)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2得到单质硫的方法来除去S02.写出该反应的化学方程式
分析:(1)硫元素的化合价有-2、0、+4、+6价,A中的S的化合价为+6价,A为三氧化硫;B为硫化氢;
(2)C中的S的化合价为+6价,H2SO4→C,发生的是复分解反应;
(3)若C为铜盐硫酸和氧化铜反应,或氢氧化铜反应,或铜和浓硫酸加热反应生成二氧化硫和硫酸铜;
(4)一定条件下用CO还原SO2得到单质硫的方法来除去S02,依据原子守恒和氧化还原反应电子守恒写出化学方程式;
(2)C中的S的化合价为+6价,H2SO4→C,发生的是复分解反应;
(3)若C为铜盐硫酸和氧化铜反应,或氢氧化铜反应,或铜和浓硫酸加热反应生成二氧化硫和硫酸铜;
(4)一定条件下用CO还原SO2得到单质硫的方法来除去S02,依据原子守恒和氧化还原反应电子守恒写出化学方程式;
解答:解:(1)A中的S的化合价为+6价且可以转化为硫酸,又可以和二氧化硫互相转化,因此A为三氧化硫;B中的硫的化合价为-2价,且为气态氢化物,因此B为硫化氢,
故答案为:SO3;H2S;
(2)C中的S的化合价为+6价,且由硫酸得到,因此可为发生复分解反应得到的硫酸盐,“H2SO4→C”转化的化学方程式可为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O,
故答案为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O;
(3)若C为铜盐硫酸和氧化铜反应,或氢氧化铜反应,或铜和浓硫酸加热反应生成二氧化硫和硫酸铜,反应的化学方程式为:H2SO4+CuO=CuSO4+H2O;
故答案为;H2SO4+CuO=CuSO4+H2O;
(4)一定条件下用CO还原SO2得到单质硫的方法来除去S02,2CO+SO2
S+2CO2 ;
故答案为:2CO+SO2
S+2CO2 ;
故答案为:SO3;H2S;
(2)C中的S的化合价为+6价,且由硫酸得到,因此可为发生复分解反应得到的硫酸盐,“H2SO4→C”转化的化学方程式可为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O,
故答案为:H2SO4+Na2CO3=Na2SO4+CO2↑+H2O;
(3)若C为铜盐硫酸和氧化铜反应,或氢氧化铜反应,或铜和浓硫酸加热反应生成二氧化硫和硫酸铜,反应的化学方程式为:H2SO4+CuO=CuSO4+H2O;
故答案为;H2SO4+CuO=CuSO4+H2O;
(4)一定条件下用CO还原SO2得到单质硫的方法来除去S02,2CO+SO2
| ||
故答案为:2CO+SO2
| ||
点评:本题考查了元素化合价分析判断,物质性质的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目