题目内容
现有六种无色溶液,它们是KCl、NaAlO2、Na2CO3、Na2S、Na2SiO3、Na2S2O3,只有一种试剂即可鉴别,这种试剂可以是 (填一种即可),将有关的现象和离子方程式填入下表空白中:
| 现象 | 离子方程式 | |
| KCl | ||
| NaAlO2 | ||
| Na2CO3 | ||
| Na2S | ||
| Na2SiO3 | ||
| Na2S2O3 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:KCl、NaAlO2、Na2CO3、Na2S、Na2SiO3、Na2S2O3阴离子各不相同,可加入盐酸鉴别,现象各不相同,KCl不反应无现象;NaAlO2先生成沉淀,盐酸过量时沉淀溶解;Na2CO3生成无色无味气体;Na2S生成臭鸡蛋气味的气体;Na2SiO3生成胶状沉淀;Na2S2O3与盐酸反应生成S和二氧化硫,生成浅黄色沉淀和刺激性气体,以此解答该题.
解答:
解:KCl、NaAlO2、Na2CO3、Na2S、Na2SiO3、Na2S2O3阴离子各不相同,可加入盐酸鉴别,现象各不相同:
KCl不反应无现象;
NaAlO2先生成沉淀,盐酸过量时沉淀溶解,离子方程式为H++AlO2-+H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O;
Na2CO3生成无色无味气体,离子方程式为CO32-+2H+=CO2↑+H2O;
Na2S生成臭鸡蛋气味的气体,离子方程式为S2-+2H+=H2S↑;
Na2SiO3生成胶状沉淀,离子方程式为SiO32-+2H+=H2SiO3↓;
Na2S2O3与盐酸反应生成S和二氧化硫,生成浅黄色沉淀和刺激性气体,离子方程式为S2O32-+2H+=SO2↑+S↓+H2O,
故答案为:盐酸;
KCl不反应无现象;
NaAlO2先生成沉淀,盐酸过量时沉淀溶解,离子方程式为H++AlO2-+H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O;
Na2CO3生成无色无味气体,离子方程式为CO32-+2H+=CO2↑+H2O;
Na2S生成臭鸡蛋气味的气体,离子方程式为S2-+2H+=H2S↑;
Na2SiO3生成胶状沉淀,离子方程式为SiO32-+2H+=H2SiO3↓;
Na2S2O3与盐酸反应生成S和二氧化硫,生成浅黄色沉淀和刺激性气体,离子方程式为S2O32-+2H+=SO2↑+S↓+H2O,
故答案为:盐酸;
| 现象 | 离子方程式 | |
| KCl | 无现象 | |
| NaAlO2 | 先生成沉淀,后溶解 | H++AlO2-+H2O=Al(OH)3↓、Al(OH)3+3H+=Al3++3H2O |
| Na2CO3 | 生成无色无味气体 | CO32-+2H+=CO2↑+H2O |
| Na2S | 生成臭鸡蛋气味的气体 | S2-+2H+=H2S↑ |
| Na2SiO3 | 生成胶状沉淀 | SiO32-+2H+=H2SiO3↓ |
| Na2S2O3 | 生成浅黄色沉淀和刺激性气体 | S2O32-+2H+=SO2↑+S↓+H2O |
点评:本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握离子方程式的书写,难度中等.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
下列有关说法正确的是( )
| A、将0.2mol/L的NH3?H2O与0.1mol/L的HCl溶液等体积混合后PH>7,则c(Cl-)>c(NH4+)>c(OH-)>c(H+) | ||
| B、已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有C(Mg2+)=C(CO32-),且C(Mg2+)?C(CO32-)═6.82×10-6 mol?L-1 | ||
C、0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:
| ||
| D、用惰性电极电解Na2SO4溶液,阳阴两极产物的物质的量之比为2:1 |
在一体积固定的密闭 容器中,进行化学反应:2X(g)+Y(s)?Z(g)+W(g),若其化学平衡常数(K)和温度(℃)的关系如下表:对该反应而言,下列说法正确的是( )
| t/℃ | 700 | 800 | 900 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.3 | 1.8 | 2.7 |
| A、该反应正反应为放热反应 |
| B、K越大,反应物的转化率越大 |
| C、温度不变,增加X的用量,K增大 |
| D、达平衡后,加入催化剂,平衡向正反应方向移动 |
下列离子方程式书写正确的是( )
| A、金属钠溶于水:2Na+2H2O=2Na++2OH-+H2↑ |
| B、Cl2与H2O反应:Cl2+H2O=2H++Cl-+ClO- |
| C、硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全一样的是( )
| A、CuCl2(CuSO4) |
| B、AgNO3(H2O) |
| C、NaCl(盐酸) |
| D、CuSO4(CuO) |
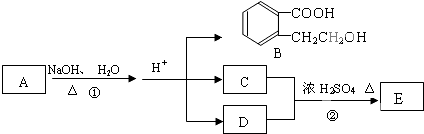
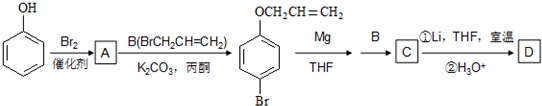
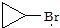 是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有
是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有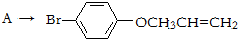 的有机反应类型:
的有机反应类型: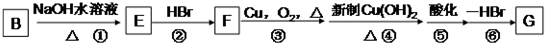
 实验设计:
实验设计: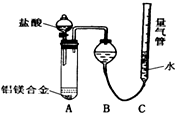 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.