题目内容
20.碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:(1)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2
若2mol CH4还原NO2至N2,整个过程中放出的热量为1734kJ,则△H2=-1160kJ/mol;
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁.
其反应如下:Fe2O3(s)+3CH4(g)?2Fe(s)+3CO(g)+6H2(g)△H>0
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g.则该段时间内CO的平均反应速率为0.012mol•L-1•min-1.
②若该反应在恒温恒压容器中进行,能表明该反应达到平衡状态的是bd(选填序号)
a.CH4的转化率等于CO的产率 b.混合气体的平均相对分子质量不变
c.v(CO)与v(H2)的比值不变 d.固体的总质量不变
③该反应达到平衡时某物理量随温度变化如图1所示,当温度由T1升高到T2时,平衡常数KA< KB(填“>”、“<”或“=”).纵坐标可以表示的物理量有哪些bc.
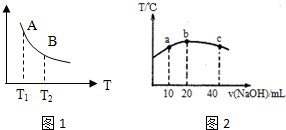
a.H2的逆反应速率 b.CH4的体积分数
c.混合气体的平均相对分子质量 d.CO的体积分数
(3)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+ )实现氨的电化学合成,从而大大提高了氮气和氢气的转化率.电化学合成氨过程的总反应式为:N2+3H2?一定条件2NH3,该过程中正极反应的方程式为N2+6H++6e-=2NH3.
(4)若往20mL 0.0lmol•L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图2所示,下列有关说法正确的是②③
①该烧碱溶液的浓度为0.02mol•L-1
②该烧碱溶液的浓度为0.01mol•L-1
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
分析 (1)CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2 ②
①+②得:2CH4(g)+4NO2(g)=2CO2(g)+4H2O(g)+2N2(g)根据盖斯定律以及热化学方程式的意义来解答;
(2)①结合题干计算铁物质的量,根据化学方程式定量关系计算甲烷消耗的物质的量,依据化学反应速率概念计算得到;
②反应达到平衡状态时,正逆反应速率相等,各组分浓度保持不变,据此分析;
③该反应是正反应气体体积增大的吸热反应,升温平衡正向移动,据此分析;
(3)燃料电池中,正极上氧化剂得电子发生还原反应;
(4)①②HNO2是弱酸,次氯酸电离是吸热反应,酸碱中和反应是放热反应,当恰好完全中和时放出热量最多,据此确定c(NaOH);
③电离吸热,温度越高电离平衡常数越大;
④当c(NaOH)较大时,可能出现:c(Na+)>c(OH-)>c(NO2-)>c(H+).
解答 解:(1)CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2 ②
根据盖斯定律得:2CH4(g)+4NO2(g)=2CO2(g)+4H2O(g)+2N2(g)△H1+△H2
而 1mol CH4还原NO2至N2,整个过程中放出的热量为867kJ,所以△H1+△H2=-1734kJ•mol-1,则△H2=-1734kJ•mol-1+574kJ•mol-1=-1160 kJ•mol-1,
故答案为:-1160kJ•mol-1;
(2)①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g的物质的量=$\frac{3.2g}{160g/mol}$=0.02mol,结合化学方程式,Fe2O3(s)+3CH4(g)═2Fe(s)+3CO(g)+6H2(g),计算反应的甲烷物质的量为0.06mol,则该段时间内CH4的平均反应速率=$\frac{\frac{0.06mol}{5L}}{1min}$=0.012mol/(L•min);
故答案为:0.012mol/(L•min);
②a.CH4的转化率与CO的产率与是否达到平衡状态无关,故a错误;
b.反应前后气体的物质的量和质量都不同,所以混合气体的平均相对分子质量不变说明反应达到平衡状态,故b正确;
c、v(CO)与v(H2)的比值始终不变,所以其不能说明反应达到平衡状态,故c错误;
d、固体的总质量不变,说明正逆反应速率相等,反应达到平衡状态,故d正确;
故答案为:bd;
③Fe2O3(s)+3CH4(g)═2Fe(s)+3CO(g)+6H2(g)△H>0,反应是气体体积增大的吸热反应,升温平衡正向移动,平衡常数增大,KA<KB;
a.H2的逆反应速率随温度的升高而增大,故a错误;
b.升温平衡正向移动,CH4的体积分数减小,故b正确;
c.升温平衡正向移动,混合气体的平均相对分子质量减小,故c正确;
d.升温平衡正向移动,CO的体积分数增大,故d错误;
故答案为:<;bc.
(3)燃料电池中,正极上氮气得电子和氢离子发生还原反应生成氨气,电极反应式为N2+6H++6e-=2NH3,故答案为:N2+6H++6e-=2NH3;
(4)①HNO2是弱酸,次氯酸电离是吸热反应,酸碱中和反应是放热反应,当恰好完全中和时放出热量最多,c(NaOH)=$\frac{0.02L×0.01mol/L}{0.020l}$=0.01mol/L;
故①错误,②正确;
③电离吸热,温度越高电离平衡常数越大,所以HNO2的电离平衡常数:b点>a点,故③正确;
④从b点到c点,当C(NaOH)较大时,可能出现:c(Na+)>c(OH-)>c(NO2-)>c(H+),故④错误;
故答案为:②③.
点评 本题综合考查学生有关热化学、化学反应速率和平衡的有关计算等知识,综合性较强,题目难度较大,注意知识的迁移应用是关键.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案| A. | 四种元素中原子半径最大的为Z | |
| B. | Y、Z、M的氢化物中,M的氢化物最稳定 | |
| C. | 四种元素最多可形成两种盐 | |
| D. | 由四种元素中的两种形成的相对分子质量最小的有机物不能发生加成反应 |
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | SO42- | HCO3- |
| 含量/mg•L-1 | 9360 | 83 | 160 | 1100 | 16000 | 1200 | 118 |
(2)下面是海水利用电渗析法获得淡水的原理图,电极为惰性电极.请分析下列问题:
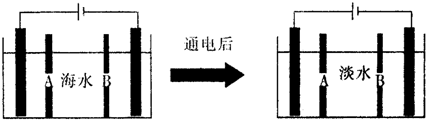
①阳离子交换膜是指B(填A或B).
②写出通电后阳极区的电极反应式:2Cl--2e-=Cl2↑.电解一段时间,阴极区会产生水垢,其成分为CaCO3和Mg(OH)2,写出生成CaCO3的离子方程式Ca2++OH-+HCO3-=CaCO3↓+H2O.
(3)水的净化与软化的区别是水的净化是用混凝剂(如明矾等)将水中悬浮物沉淀下来,而水的软化是除去水中的钙离子和镁离子;离子交换法是软化水的常用方法,聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式CH2=CHCOONa.
(4)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3,吸收80g Br2时转移的电子为$\frac{5}{6}$mol.
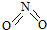 和
和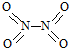 .已知:N-N键能为167kJ•mol-1,NO2中N=O键能为466kJ•mol-1,N2O4中N=O键能为438.5kJ•mol-1.
.已知:N-N键能为167kJ•mol-1,NO2中N=O键能为466kJ•mol-1,N2O4中N=O键能为438.5kJ•mol-1.(1)写出N2O4转化为NO2的热化学方程式:N2O4(g)=2NO2(g)△H=+57kJ•mol-1.
(2)在100℃时,将0.40mol的NO2气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
②n3=n4(填“>”、“<”或“=”),反应2NO2?N2O4的平衡常数K的数值为2.8(精确到小数点后两位),升高温度后,该反应的平衡常数K将减小(填“增大”、“减小”或“不变”).
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度是0.10mol•L-1.
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料.电池的总反应为4NH3(g)+3O2(g)=2N2(g)+6H2O(g),则该燃料电池的负极反应式:2NH3+6OH--6e-=N2+6H2O.
①淀粉 ②纤维素 ③油脂 ④蔗糖 ③聚乙烯.
| A. | ①②③ | B. | ①②④ | C. | ①②⑤ | D. | 全部 |
| A. | 高分子分离膜 | B. | 隐形眼镜 | C. | 人造丝 | D. | 人造骨酪 |
| A. | 二甲苯 | B. | 丁醇 | C. | 一氯丁烯 | D. | 二氯丙烷 |
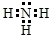 ;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;
;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;