题目内容
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 1mol 18O含有的中子数为10NA | |
| B. | 22.4L甲烷气体中所含分子数目为NA | |
| C. | 1L 0.1mol•L-1NH4Cl 溶液中NH4+数目为 0.1NA | |
| D. | 1L pH=1的醋酸溶液中,CH3COOH分子的数目为0.1NA |
分析 A、18O中含10个中子;
B、甲烷所处的状态不明确;
C、NH4+是弱碱阳离子,在溶液中会水解;
D、醋酸是弱酸,只能部分电离.
解答 解:A、18O中含10个中子,故1mol18O中含10mol中子即10NA个,故A正确;
B、甲烷所处的状态不明确,故其物质的量和分子个数无法计算,故B错误;
C、NH4+是弱碱阳离子,在溶液中会水解,故溶液中的铵根离子的个数小于0.1NA个,故C错误;
D、醋酸是弱酸,只能部分电离,故1LpH=1的醋酸溶液中氢离子个数为0.1NA个,但醋酸分子个数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
12.下列离子方程式中,正确的是( )
| A. | 钠放入水中 Na+H2O═Na++OH-+H2↑ | |
| B. | 电解饱和食盐水 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | 实验室用氯化铝溶液和氨水制氢氧化铝 Al3++3OH-═Al(OH)3↓ | |
| D. | 向碳酸氢铵溶液中加入足量氢氧化钠溶液 HCO3-+OH-═CO32-+H2O |
13.下列叙述正确的是( )
| A. | NaCl的摩尔质量是58.5g | |
| B. | 将40g氢氧化钠溶解在1L水中可配制物质的量浓度为1mol/L的氢氧化钠溶液 | |
| C. | 气体摩尔体积指lmol任何气体所占的体积约为22.4L | |
| D. | 10毫升1mol/L氯化铝溶液与50毫升3mol/L氯化钠溶液中所含氯离子物质的量浓度相等 |
10.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 11.2L NH3中含有的氢原子数为1.5NA | |
| B. | 0.2mol/L AlCl3溶液含有0.2NA个Al3+ | |
| C. | 常温常压下,18g水的原子数为3NA | |
| D. | O2与O3的混合物32g,含有分子数为NA |
17.除去下列物质中的少量杂质(括号内),选用的试剂和分离方法不能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 粗苯甲酸(泥沙等) | 水 | 重结晶 |
| B | 甲烷(乙烯) | 高锰酸钾酸性溶液 | 洗气 |
| C | 乙炔(硫化氢) | 硫酸铜溶液 | 洗气 |
| D | 溴苯(溴) | 稀氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
7.将氯气分别通入下列溶液中,由实验现象得出的结论正确的是( )
| 选项 | 氯气通入下列溶液中 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液 | 变红 | 氯气具有还原性 |
| B | 滴有酚酞的NaOH溶液 | 褪色 | 氯气具有漂白性 |
| C | 紫色石蕊溶液 | 先变红后褪色 | 氯气具有酸性、漂白性 |
| D | 少量氯气通入大量水中 | 溶液pH<7 呈浅黄绿色 | 氯气与水反应生成酸性物质, 且该反应为可逆反应 |
| A. | A | B. | B | C. | C | D. | D |
14.在pH=13的无色溶液中能大量共存的是( )
| A. | NH4+、SO42-、Cl- | B. | Al3+、N03-、Cl- | C. | K+、MnO4-、SO42- | D. | Na+、CO32-、NO3- |
11.今有分别含①HSO3-;②两个原子核10e-的阴离子;③SO32-;④HS-;⑤26M2+;⑥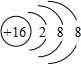 离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
 离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )
离子的六种溶液,向每种溶液中分别加入少量氢氧化钠固体、少量浓盐酸,几滴酸性高锰酸钾溶液,其离子数目都减少的是( )| A. | ①②④ | B. | ②③⑤ | C. | ①④ | D. | ③⑤⑥ |
20.下列化学反应可以设计成原电池的是( )
| A. | 2H2+O2═2H2O | B. | H++OH-═H2O | ||
| C. | .CaCO3═CaO+CO2↑ | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |