题目内容
设N0为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、12g石墨烯(单层石墨)中含有六元环的个数为0.5N0 |
| B、1.0L1.0mo1?L-1的NaNO3水溶液中含有的氧原子数为3N0 |
| C、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 N0 |
| D、1 mol的羟基与1 mol的氢氧根离子所含电子数均为9 N0 |
考点:阿伏加德罗常数
专题:
分析:A.石墨烯中,每个碳原子被3个六元环共用,根据均摊法计算出12gC能够形成的六元环的数目;
B.硝酸钠溶液中,溶剂水中也含有氧原子;
C.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目;
D.羟基中含有9个电子,氢氧根离子含有10个电子.
B.硝酸钠溶液中,溶剂水中也含有氧原子;
C.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目;
D.羟基中含有9个电子,氢氧根离子含有10个电子.
解答:
解:A.12g石墨烯中含有1molC,每个碳原子被3个六元环共用,每个六元环中含有的碳原子数目为:
×6=2,所以1molC原子形成的六元环的物质的量为:
=0.5mol,含有六元环的个数是0.5N0,故A正确;
B.在硝酸钠溶液中,由于水中也含有氧原子,则无法计算溶液中含有氧原子的数目,故B错误;
C.没有告诉氢氧化钠溶液的体积,无法计算溶液中含有氢氧根离子的物质的量,故C错误;
D.1mol氢氧根离子中含有10mol电子,1mol羟基中含有9mol电子,二者含有的电子数不相同,故D错误;
故选A.
| 1 |
| 3 |
| 1mol |
| 2 |
B.在硝酸钠溶液中,由于水中也含有氧原子,则无法计算溶液中含有氧原子的数目,故B错误;
C.没有告诉氢氧化钠溶液的体积,无法计算溶液中含有氢氧根离子的物质的量,故C错误;
D.1mol氢氧根离子中含有10mol电子,1mol羟基中含有9mol电子,二者含有的电子数不相同,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意水中含有氧原子,选项A为难点,需要明确石墨烯的结构的结构及均摊法的应用方法.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
下列各图所反映的措施中,目的是为了加快其化学反应速率的是( )
A、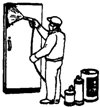 铁门表面喷漆 |
B、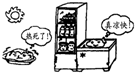 冰箱保存食物 |
C、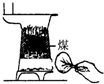 扇子扇煤炉火 |
D、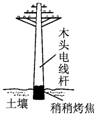 |
将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是( )
| A、Ca(OH)2的溶解度、溶剂的质量 |
| B、溶液中溶质的质量分数 |
| C、溶液的质量、水的电离平衡 |
| D、溶液中Ca2+的数目、溶液中Ca2+的浓度 |
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
| A、电子数之比1:1 |
| B、体积比16:11 |
| C、密度比16:11 |
| D、氧原子数之比为1:1 |
设NA代表阿伏加德罗常数的值,下列说法不正确的是( )
| A、23gNa变为Na+时失去的电子数为NA |
| B、17g OH-所含的电子数为9NA |
| C、标准状况下,11.2LNH3所含的分子数目为0.5NA |
| D、含71g Na2SO4的溶液中所含Na+离子数目为NA |
下列反应的离子方程式正确的是( )
| A、氢氧化钡中加入稀硫酸:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
| B、氧化铜溶于稀硫酸:2H++CuO=Cu2++H2O |
| C、碳酸钙溶于盐酸:CO32-+2H+=CO2↑+H2O |
| D、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
经测定:常温、常压下的一瓶气体中只含有C、O两种元素,通常情况下,这瓶气体不可能是( )
| A、一种纯净的化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物的混合物 |
| D、两种单质的混合物 |
某CaCl2样品中可能含有FeCl3、MgCl2、NaCl和Na2CO3中的一种或两种.将11.1克此样品溶于水得无色溶液,加入足量的AgNO3溶液得沉淀29.7克,由此可知所含杂质的正确结论是( )
| A、一定无Na2CO3,可能有FeCl3 |
| B、可能有Na2CO3和NaCl |
| C、一定有MgCl2,可能有NaCl |
| D、一定有NaCl |