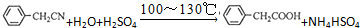题目内容
4.下列有关沉淀溶解平衡的说法中不正确的是( )| A. | 难溶电解质在水中存在沉淀溶解平衡,且是一种动态平衡 | |
| B. | Ksp只与难溶电解质的性质和温度有关,而与沉淀的量和离子浓度无关 | |
| C. | 在一定温度下的BaSO4饱和溶液中加入少量BaCl2固体,BaSO4的Ksp减少 | |
| D. | 当阴、阳离子个数比相同时,难溶电解质的Ksp数值越大,溶解能力越强 |
分析 难溶电解质的溶解平衡为动态平衡,Ksp为平衡常数,只受温度的影响,Ksp越大,说明越易溶解,以此解答该题.
解答 解:A.难溶电解质在溶液中达到沉淀溶解平衡时生成沉淀的速率和沉淀溶解的速率相等,且不等于零,即沉淀溶解平衡是一种动态平衡,故A正确;
B.Ksp是温度的常数,只随温度改变而改变,不同物质的溶解能力不同,与物质本身的性质有关,故B正确;
C.溶度积只受温度的影响,故C错误;
D.难溶电解质的Ksp数值越大,可说明越易溶于水,故D正确.
故选C.
点评 本题考查难溶电解质的溶解平衡及沉淀转化的本质,为高频考点,侧重于学生的分析能力的考查,注意Ksp是温度的常数,只随温度改变而改变,题目难度不大.

练习册系列答案
相关题目
2. 人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
 人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )| A. | A为电源的负极 | |
| B. | 电解结束后,阴极室溶液的pH与电解前相比将不变 | |
| C. | 阳极室中发生的电极反应为2H++2e-═H2↑ | |
| D. | 若两极共收集到气体13.44 L(标准状况),则除去的尿素为18g(忽略气体的溶解) |
3.微量元素在人体内含量极少,但它们对于维持生命活动,促进人体健康生长和发育都有极其重要的作用.下列元素中,若缺乏严重会导致智力损害的是( )
| A. | 钙元素 | B. | 碘元素 | C. | 铁元素 | D. | 钠元素 |
12.已知Ksp(AB2)=4.2×10-8,Ksp(AC)=3.0×10-15.在AB2、AC均为饱和的混合液中,测得c(B-)=1.6×10-3 mol•L-1,则溶液中c(C2-)为( )
| A. | 1.8×10-13 mol•L-1 | B. | 7.3×10-13 mol•L-1 | ||
| C. | 2.3 mol•L-1 | D. | 3.7 mol•L-1 |
19.用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“0”或“0”刻度线稍下,并记下读数;④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;⑤用标准液滴定至终点,记下滴定管液面读数.⑥重复以上滴定操作2-3次.请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果偏大 (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果无影响(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视锥形瓶中溶液颜色变化;判断到达滴定终点的依据是:锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(4)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是AB
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:0.1626mol/L.
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“0”或“0”刻度线稍下,并记下读数;④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;⑤用标准液滴定至终点,记下滴定管液面读数.⑥重复以上滴定操作2-3次.请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果偏大 (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果无影响(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视锥形瓶中溶液颜色变化;判断到达滴定终点的依据是:锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(4)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是AB
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
| 滴定 次数 | 盐酸体积 (mL) | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:0.1626mol/L.
9.已知25℃时,电离常数Ka(HF)=3.6×10-4mol•L-1,溶度积常数Ksp(CaF2)=1.46×10-10,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10一16.下列说法正确的是( )
| A. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| B. | 向1 L0.2 mol•L-1 HF溶液中加入1 L 0.2 mol•L-1 CaCl2溶液,没有沉淀产生 | |
| C. | AgCl不溶于水,不能转化为AgI | |
| D. | 常温AgCl若在NaI溶液中开始转化为AgI,NaI浓度必须不低于$\frac{1}{\sqrt{1.8}}$×10-11 mol•L-1 |
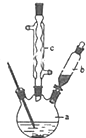
16.己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图为: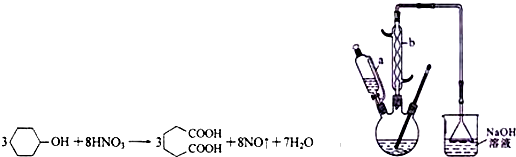
实验步骤如下:
Ⅰ.在三口烧瓶中加入16mL50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色
气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管(或冷凝管),使用时要从下口(填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是平衡滴液漏斗与三口烧瓶内的气压,使环己醇能够顺利流下.
(2)本实验所用50%的硝酸的物质的量浓度为10.4mol/L;NaOH溶液的作用是吸收NO2,防止污染空气.
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三口烧瓶置于冷水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冷水和苯洗涤晶体.
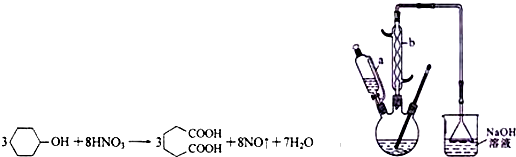
| 物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
Ⅰ.在三口烧瓶中加入16mL50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色
气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管(或冷凝管),使用时要从下口(填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是平衡滴液漏斗与三口烧瓶内的气压,使环己醇能够顺利流下.
(2)本实验所用50%的硝酸的物质的量浓度为10.4mol/L;NaOH溶液的作用是吸收NO2,防止污染空气.
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三口烧瓶置于冷水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冷水和苯洗涤晶体.
13.聚合氯化铝(PAC)是常用于水质净化的无机高分子混凝剂,其化学式可表示为[Al2(OH)nCl6-n]m(n<6,m为聚合度).PAC常用高温活化后的高岭土(主要化学组成为Al2O3、SiO2、Fe2O3)进行制备,工艺流程如下图所示:
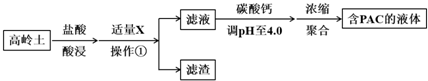
(1)盐酸酸浸所涉及反应的离子方程式是6H++Al2O3═2Al3++3H2O、6H++Fe2O3═2Fe3++3H2O.
(2)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释加入X的主要目的:调节溶液pH至Fe3+完全沉淀,滤渣中主要含有物质的化学式是Fe(OH)3、SiO2.
(3)已知:生成液体PAC的反应为2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+.
用碳酸钙调节溶液的pH时,要严控pH的大小,pH偏小或偏大液体PAC的产率都会降低.请解释pH偏小液体PAC产率降低的原因:pH偏小时,抑制平衡2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+ 正向移动生成PAC.
(4)浓缩聚合得到含PAC的液体中铝的各种形态主要包括:
Ala--Al3+单体形态铝
Alb--[Al2(OH)nCl6-n]m聚合形态铝
Alc--Al(OH)3胶体形态
图1为Al各形态百分数随温度变化的曲线;图2为含PAC的液体中铝的总浓度AlT随温度变化的曲线.

①50-90℃之间制备的液体PAC中,聚合形态铝含量最多.
②当T>80℃时,AlT明显降低的原因是温度升高,导致液体PAC向Al(OH)3沉淀转化.

(1)盐酸酸浸所涉及反应的离子方程式是6H++Al2O3═2Al3++3H2O、6H++Fe2O3═2Fe3++3H2O.
(2)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 1.5 |
| 完全沉淀时 | 4.7 | 2.8 |
根据表中数据解释加入X的主要目的:调节溶液pH至Fe3+完全沉淀,滤渣中主要含有物质的化学式是Fe(OH)3、SiO2.
(3)已知:生成液体PAC的反应为2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+.
用碳酸钙调节溶液的pH时,要严控pH的大小,pH偏小或偏大液体PAC的产率都会降低.请解释pH偏小液体PAC产率降低的原因:pH偏小时,抑制平衡2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+ 正向移动生成PAC.
(4)浓缩聚合得到含PAC的液体中铝的各种形态主要包括:
Ala--Al3+单体形态铝
Alb--[Al2(OH)nCl6-n]m聚合形态铝
Alc--Al(OH)3胶体形态
图1为Al各形态百分数随温度变化的曲线;图2为含PAC的液体中铝的总浓度AlT随温度变化的曲线.

①50-90℃之间制备的液体PAC中,聚合形态铝含量最多.
②当T>80℃时,AlT明显降低的原因是温度升高,导致液体PAC向Al(OH)3沉淀转化.
 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱之一.下面是它的一种实验室合成路线: