题目内容
12.将0.1 mol•L-1的FeCl3溶液与0.lmol•L-1的KI溶液等体积混合充分反应:2FeCl3+2KI?2FeCl2+2KCl+I2,下列能证明该反应存在一定的反应限度的是( )| A. | 溶液中能检测到Fe2+ | B. | 溶液中能检测到I2 | ||
| C. | 溶液中能检测到Fe3+ | D. | 溶液中能检测到Cl- |
分析 通过检验少量的反应物是否剩余来判断KI溶液和FeCl3溶液反应是否存在一定的反应限度.
解答 解:将0.1 mol•L-1的FeCl3溶液与0.lmol•L-1的KI溶液等体积混合充分反应:2FeCl3+2KI?2FeCl2+2KCl+I2,则两种反应物按1:1投入,又按1:1反应,所以只要能检验出Fe3+或者I-剩余,即可证明该反应存在一定的反应限度,故选:C.
点评 本题考查了化学反应可逆性的检验,难度不大,抓住检验少量的反应物有剩余即可,试题侧重考查学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
2.铝热反应是铝的一个重要性质,该性质用途十分广泛.“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”.已知:Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如表:
I.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?合理(填“合理”或“不合理”).
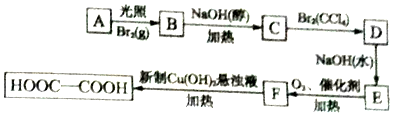
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是B(填序号).
A、浓硫酸 B、稀硫酸 C、稀硝酸 D、氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入6mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
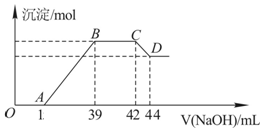
(1)依题意,请写出熔融物中铁与该稀的硝酸反应的离子方程式:8Fe+30H++3NO3-═8 Fe3++3NH4++9 H2O
(2)图中OA段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.
(3)在BC段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O;
(4)熔融物中铝元素的物质的量为0.012mol.
(5)B点对应的沉淀的物质的量为0.048mol,A点对应的氢氧化钠溶液的体积为15mL.
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
| 沸点/℃ | 2 467 | 2 980 | 2 750 | - |
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是NaOH溶液,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是B(填序号).
A、浓硫酸 B、稀硫酸 C、稀硝酸 D、氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入6mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:

(1)依题意,请写出熔融物中铁与该稀的硝酸反应的离子方程式:8Fe+30H++3NO3-═8 Fe3++3NH4++9 H2O
(2)图中OA段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.
(3)在BC段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为NH4++OH-═NH3•H2O;
(4)熔融物中铝元素的物质的量为0.012mol.
(5)B点对应的沉淀的物质的量为0.048mol,A点对应的氢氧化钠溶液的体积为15mL.
20.下列分子式能表示的物质只有一种的是( )
| A. | C5H10 | B. | CH4O | C. | C7H8O | D. | C2H4Cl2 |
7.不能作为判断氯、磷两种元素非金属性强弱的依据的是( )
| A. | 氧化性:Cl2>红磷 | B. | 单质沸点:红磷>C12 | ||
| C. | 氢化物稳定性:HC1>PH3 | D. | 酸性:HClO4>H3PO4 |
17.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 乙烯是化学物质,不可用作水果的催熟剂 | |
| B. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| C. | 石油是混合物,经分馏后得到汽油、煤油和柴油等纯净物 | |
| D. | 汽油与水互不相溶,但不可以用裂化汽油萃取溴水中的溴 |
4.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 常温下遇铁都发生钝化 | B. | 常温下都能与铜反应产生氢气 | ||
| C. | 露置于空气中,溶液质量均不变 | D. | 露置于空气中,溶液浓度均不变 |
1.《诗词大会》不仅弘扬了中国传统文化,还蕴含了许多化学知识.下列说法不合理的是( )
| A. | 李白的诗句:“日照香炉生紫烟,遥看瀑布挂前川.”生紫烟包含了物理变化 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 | |
| C. | 唐末五代时期丹学著作《元妙道要略》中有云“以硫黄、雄黄台硝石并蜜烧之;焰起,烧手面及烬屋舍者”.描述的是丹药的制作过程 | |
| D. | 古剑沈卢“以济钢为刃,柔铁为茎干,不尔则多折断”. 济钢指的是铁的合金 |