题目内容
甲烷与氧气按一定比例混合后点燃生成CO、CO2和H2O,生成物总质量为18.4g,通过浓硫酸后,质量减少9g,求:
(1)原混合气体中甲烷和氧气的体积比为 ;
(2)写出这一燃烧反应的化学方程式为 .
(1)原混合气体中甲烷和氧气的体积比为
(2)写出这一燃烧反应的化学方程式为
考点:有关混合物反应的计算
专题:计算题
分析:(1)浓硫酸吸收水,二氧化碳和CO的质量为18.4g-9g=9.4g,则n(H2O)=
=0.5mol,根据氢原子守恒知,n(H)=2n(H2O)=2×0.5mol=1mol,根据甲烷的化学式知n(C)=
n(H)=0.25mol,
根据C原子守恒知,n(CH4)=n(C)=0.25mol,根据氧原子守恒得n(O2)=
=0.45mol,相同条件下,不同气体的物质的量之比等于其体积之比;
(2)根据碳原子守恒计算二氧化碳、一氧化碳的物质的量,根据各个物理量之间的物质的量之比写出该反应方程式.
| 9g |
| 18g/mol |
| 1 |
| 4 |
根据C原子守恒知,n(CH4)=n(C)=0.25mol,根据氧原子守恒得n(O2)=
| 18.4g-0.25mol×16g/mol |
| 32g/mol |
(2)根据碳原子守恒计算二氧化碳、一氧化碳的物质的量,根据各个物理量之间的物质的量之比写出该反应方程式.
解答:
解:(1)浓硫酸吸收水,二氧化碳和CO的质量为18.4g-9g=9.4g,则n(H2O)=
=0.5mol,根据氢原子守恒知,n(H)=2n(H2O)=2×0.5mol=1mol,根据甲烷的化学式知n(C)=
n(H)=0.25mol,
根据C原子守恒知,n(CH4)=n(C)=0.25mol,根据氧原子守恒得n(O2)=
=0.45mol,相同条件下,不同气体的物质的量之比等于其体积之比,所以V(CH4):V(O2)=0.25mol:0.45mol=5:9,
故答案为:5:9;
(2)设二氧化碳的物质的量为x,CO的物质的量为y,
则
解得
则CH4、O2、CO2、CO、H2O的物质的量之比=0.25:0.45:0.15:0.1:0.5=5:9:3:2:10,其物质的量之比等于其计量数之比,所以该反应方程式为5CH4+9O2
3CO2+2CO+10H2O,
故答案为:5CH4+9O2
3CO2+2CO+10H2O.
| 9g |
| 18g/mol |
| 1 |
| 4 |
根据C原子守恒知,n(CH4)=n(C)=0.25mol,根据氧原子守恒得n(O2)=
| 18.4g-0.25mol×16g/mol |
| 32g/mol |
故答案为:5:9;
(2)设二氧化碳的物质的量为x,CO的物质的量为y,
则
|
|
则CH4、O2、CO2、CO、H2O的物质的量之比=0.25:0.45:0.15:0.1:0.5=5:9:3:2:10,其物质的量之比等于其计量数之比,所以该反应方程式为5CH4+9O2
| ||
故答案为:5CH4+9O2
| ||
点评:本题考查了物质的量的计算,根据原子守恒进行有关计算,题目难度中等,难点是氧气物质的量的计算.

练习册系列答案
相关题目
某有机物的键线式为 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A、不溶于水 |
| B、属于芳香族化合物 |
| C、在加热和催化剂作用下,最多能和4mol H2反应 |
| D、既能发生氧化反应也能发生加聚反应 |
把6.72L NO2气体,依次通过下列3个分别装有足量①NaHCO3饱和溶液,②浓H2SO4,③Na2O2的装置后,用排水法把残留气体收集到集气瓶中并得到200mL溶液,下列说法错误的是(气体体积均在标况下测定)( )
| A、最后所得溶液的物质的量浓度是0.33mol/L |
| B、通过装置①②后气体体积仍为6.72L |
| C、通过装置③后所得气体呈红棕色 |
| D、集气瓶中收集到0.025mol O2 |
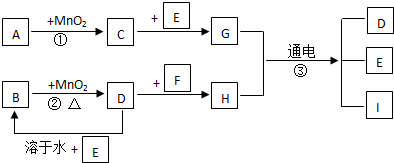
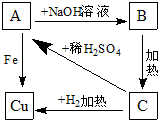 A、B、C和铜关系如图:
A、B、C和铜关系如图: