题目内容
在一定条件下在固定容器中进行的可逆反应2M(g)+N(g)?Q(g)△H>0,达到平衡状态,若升高温度,则对于该混合气体下列说法正确的是( )
| A、密度增大 |
| B、平均相对分子质量增大 |
| C、总分子数增大 |
| D、平衡逆向移动 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:依据化学平衡影响因素分析,结合平衡移动原理判断进行方向,利用进行方向和反应特征分析选项.
解答:
解:2M(g)+N(g)?Q(g)△H>0,反应是气体体积减小的吸热反应,升温,平衡正向进行,
A、反应前后气体质量不变,体积不变,升温反应正向进行,但密度不变,故A错误;
B、反应前后气体质量不变,物质的量变化,升温平衡正向进行,气体物质的量减小,平均相对分子质量增大,故B正确;
C、升温平衡正向进行,气体物质的量减小,总分子数减小,故C错误;
D、反应是气体体积减小的吸热反应,升温,平衡正向进行,故D错误;
故选B.
A、反应前后气体质量不变,体积不变,升温反应正向进行,但密度不变,故A错误;
B、反应前后气体质量不变,物质的量变化,升温平衡正向进行,气体物质的量减小,平均相对分子质量增大,故B正确;
C、升温平衡正向进行,气体物质的量减小,总分子数减小,故C错误;
D、反应是气体体积减小的吸热反应,升温,平衡正向进行,故D错误;
故选B.
点评:本题考查了化学平衡影响因素分析判断,主要是反应特征和移动方向的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
深秋及寒冬的清晨,我们安庆市经常出现大雾天气,雾中小液滴直径范围是( )
| A、小于1 nm |
| B、在1~100 nm间 |
| C、大于100 nm |
| D、无法确定 |
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质 |
| B、用渗析的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
下列反应的离子方程式正确的是( )
| A、氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 |
| B、金属钠跟水反应Na+H2O═Na++OH-+H2↑ |
| C、碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、澄清的石灰水跟盐酸反应H++OH-═H2O |
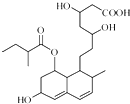 普伐他汀是一种调节血脂的药物其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述不正确的是( )
普伐他汀是一种调节血脂的药物其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述不正确的是( )| A、不能与FeCl3溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加成、取代、消去、氧化等反应 |
| D、在一定条件下,1mol该物质最多可与1molNaOH反应 |
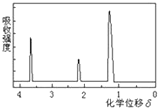
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是( )

| A、C2H5OH |
B、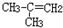 |
| C、CH3CH2CH2COOH |
D、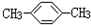 |
下列物质不能和氯气发生取代反应的是( )
| A、CH3Cl |
| B、CH2Cl2 |
| C、CHCl3 |
| D、CCl4 |
下列叙述中,正确的是( )
| A、在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B、得电子越多的氧化剂,其氧化性就越强 |
| C、反应前各原子的物质的量之和一定等于反应后各原子的物质的量之和 |
| D、溶液稀释前溶质的物质的量一定等于溶液稀释后溶质的物质的量 |
根据以下4个反应,确定Br-、I-、H2S、SO2的还原性由强到弱的顺序是( )
①H2S+I2=S↓+2I-+2H+ ②SO2+2H2S=3S+2H2O
③2I-+Br2=I2+2Br- ④SO2+I2+2H2O=H2SO4+2HI.
①H2S+I2=S↓+2I-+2H+ ②SO2+2H2S=3S+2H2O
③2I-+Br2=I2+2Br- ④SO2+I2+2H2O=H2SO4+2HI.
| A、H2S>SO2>I->Br- |
| B、I->Br->SO2>H2S |
| C、H2S>I->Br->SO2 |
| D、I->Br->H2S>SO2 |