题目内容
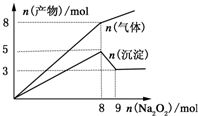 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示.则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示.则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )分析:将Na2O2先与水反应生成氢氧化钠和氧气,OH-再Al3+、Mg2+、NH4+与反应,由图表可知,加入8mol Na2O2时,气体为氨气和氧气,且NH4+恰好反应完,沉淀为氢氧化镁和氢氧化铝,且Al3+、Mg2+恰好反应完,此时溶液中Al3+、Mg2+、NH4+被Na+代替,即Al3+、Mg2+、NH4+所带的总电量等于Na+所带的总电量,据此排除解答.
解答:解:加入8mol Na2O2时,根据钠原子守恒,可知n(Na+)=2n(Na2O2)=2×8mol=16mol,Na+所带的总电量相当于16mol×1=16mol.
A、Al3+、Mg2+、NH4+所带的总电量相当于2mol×3+3mol×2+8mol×1=20mol,故A错误;
B、Al3+、Mg2+、NH4+所带的总电量相当于3mol×3+2mol×2+8mol×1=21mol,故B错误;
C、Al3+、Mg2+、NH4+所带的总电量相当于2mol×3+3mol×2+4mol×1=16mol,故C正确;
D、Al3+、Mg2+、NH4+所带的总电量相当于3mol×3+2mol×2+4mol×1=17mol,故D错误.
故选C.
A、Al3+、Mg2+、NH4+所带的总电量相当于2mol×3+3mol×2+8mol×1=20mol,故A错误;
B、Al3+、Mg2+、NH4+所带的总电量相当于3mol×3+2mol×2+8mol×1=21mol,故B错误;
C、Al3+、Mg2+、NH4+所带的总电量相当于2mol×3+3mol×2+4mol×1=16mol,故C正确;
D、Al3+、Mg2+、NH4+所带的总电量相当于3mol×3+2mol×2+4mol×1=17mol,故D错误.
故选C.
点评:本题如按图表计算是一个计算量比较大的题目,容易出错,本解法采用Al3+、Mg2+、NH4+所带的总电量等于Na+所带的总电量,据此排除解答,简化解题过程,排除法是解答选择题最常用方法之一.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
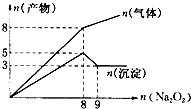 将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH4+的物质的量分别为( )| A、2 mol、3 mol、8 mol | B、3 mol、2 mol、8 mol | C、2 mol、3 mol、4 mol | D、3 mol、2 mol、4 mol |
将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如下图所示,则原混合液中Al3+、Mg2+、NH4+的物质的量分别是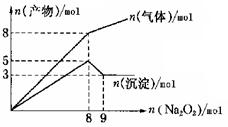
| A.2mol、3mol、4mol | B.2mol、3mol、8mol |
| C.3mol、2mol、8mol | D.3mol、2mol、4mol |
 (2013?防城港二模)某混合溶液中,可能大量含有的离子如下表:
(2013?防城港二模)某混合溶液中,可能大量含有的离子如下表: