题目内容
17.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtW ü thrich等人为此获得2002年诺贝尔化学奖.下面有关13C、15N叙述正确的是( )| A. | 13C与15N有相同的中子数 | B. | 13C的质子数为13 | ||
| C. | 15N与14N互为同位素 | D. | 15N的核外电子数与中子数相同 |
分析 A.中子数=质量数-质子数;
B.13C的质子数为6;
C.质子数相同、中子数不同的原子,互为同位素;
D.15N的核外电子数为7,中子数=15-7=8.
解答 解:A.中子数=质量数-质子数,则13C与15N的中子数分别为13-6=7、15-7=8,中子数不同,故A错误;
B.13C的质子数为6,质量数为13,故B错误;
C.15N与14N的质子数均为7、中子数分别为8、7,则15N与14N互为同位素,故C正确;
D.15N的核外电子数为7,中子数=15-7=8,核外电子数与中子数不相同,故D错误;
故选C.
点评 本题考查原子结构与性质,为高频考点,把握原子中的数量关系、核素的表示方法及不同位置数字的意义为解答关键,侧重分析与应用能力的考查,注意原子中数量关系,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
8.某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为放热反应,中和反应都是放热反应,其实质是酸电离出的H+与碱电离出的OH-结合生成弱电解质水:H++OH-═H2O.
5.下列各组微粒互为同位素的是( )
| A. | 1H和2H | B. | 14C和14N | C. | 37Cl和37Cl - | D. | 56Fe2+和56Fe3+ |
12.下列各组物质中,一定互为同系物的是( )
| A. | C2H4和C8H8 | B. | 乙烷和己烷 | C. | 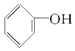 和 和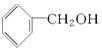 | D. | HCHO、CH3COOH |
2.向溶液中分别通入足量的相应气体后,下列各组离子还能大量存在的是( )
| A. | 氯气:K+、Na+、SiO32-、NO3- | B. | 二氧化硫:Na+、NH4+、SO32-、C1- | ||
| C. | 硫化氢:H+、K+、MnO4-、SO42- | D. | 氨气:K+、Na+、AlO2-、CO32- |
20.溴水中存在着如下的平衡:Br2+H2O?HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是( )
| A. | 加压 | B. | 加入NaF晶体 | C. | 通入SO2气体 | D. | 加入NaI晶体 |
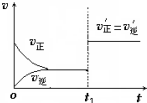 在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).
在其他条件不变的情况下,降低温度平衡向正反应方向移动,为放热反应(选填“吸热”、“放热”).如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是c(填写编号).