题目内容
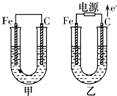 甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:(1)甲池为
(2)乙为电解池,根据图上的电子流向可以判断出C为阳极,该电极上的反应类型为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲池属于原电池,铁易失电子作负极,碳作负极,正极上氧气得电子发生还原反应;
(2)乙池属于电解池,根据电子流向知,C电极为阳极,铁电极为阴极,阴极上发生还原反应.
(2)乙池属于电解池,根据电子流向知,C电极为阳极,铁电极为阴极,阴极上发生还原反应.
解答:
解:(1)甲装置是将化学能转化为电能的装置,为原电池,铁易失电子作负极,碳作正极,在NaCl溶液中,正极上氧气得电子发生还原反应,为吸氧腐蚀,电极反应式为2H2O+O2+4e-=4OH-,
故答案为:原电池;负;吸氧;O2;4OH-;
(2)乙池有外接电源,属于电解池,根据电子流向知,C为阳极,发生氧化反应,Fe为阳极时,Fe失电子生成亚铁离子,电极反应式为:Fe-2e-═Fe2+,
故答案为:氧化反应;Fe-2e-═Fe2+.
故答案为:原电池;负;吸氧;O2;4OH-;
(2)乙池有外接电源,属于电解池,根据电子流向知,C为阳极,发生氧化反应,Fe为阳极时,Fe失电子生成亚铁离子,电极反应式为:Fe-2e-═Fe2+,
故答案为:氧化反应;Fe-2e-═Fe2+.
点评:本题考查了金属的腐蚀,明确原电池和电解池原理是解本题关键,再结合离子放电顺序及物质间的关系来分析解答,难度不大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A、K+、Cu2+、Na+、Cl- |
| B、SO42-、Na+、NO3-、CO32- |
| C、Na+、H+、NO3-、SO42- |
| D、Al3+、Na+、Cl-、SO42- |
增大压强对下列平衡没有影响的是( )
| A、N2(g)+3H2(g)?2NH3(g)△H<0 |
| B、2NO(g)+2CO(g)?2CO2(g)+N2(g)△H<0 |
| C、2HI(g)?H2(g)+I2(g)△H>0 |
| D、2NO2(g)?2NO(g)+O2(g)△H>0 |
下列说法正确的是( )
| A、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
| B、淀粉和纤维素都可以作为工业上生产葡萄糖的原料 |
| C、油脂的水解反应,都是皂化反应 |
| D、蔗糖是高分子化合物,其水解产物能发生银镜反应 |
下列物质属于电解质的是( )
| A、铁 | B、氯化钠 | C、酒精 | D、稀盐酸 |
下列有机物中含有两种官能团的是( )
| A、CH2═CHCl |
B、 |
| C、CH2Cl-CH2-CH2Cl |
D、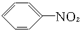 |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、0.1mol?L-1Mg(NO3)2溶液中含有0.2nA个NO3- |
| B、8g CH4中含有10nA个电子 |
| C、常温常压下,22.4L O3中含有3nA个氧原子 |
| D、28g C2H4中含有2nA个碳原子 |
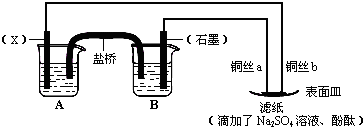
 金属腐蚀的电化学原理可用如图模拟.
金属腐蚀的电化学原理可用如图模拟.