题目内容
2.古代造纸工艺中使用的某种物质存在副作用,它易导致纸张发生酸性腐蚀,使纸张变脆,易破损.该物质是( )| A. | 熟石灰 | B. | 草木灰 | C. | 明矾 | D. | 漂白粉 |
分析 依据题意可知该物质导致纸张发生酸性腐蚀,说明该物质溶液显酸性,据此分析解答.
解答 解:A.熟石灰为氢氧化钙,显碱性,故A不选;
B.草木灰主要成分为碳酸钾,水解显碱性,故B不选;
C.明矾[KAl(SO4)2•12H2O]中铝离子水解,Al3++3H2O?Al(OH)3+3H+,产生氢离子,溶液显酸性,故C选;
D.漂白粉中次氯酸钙为强碱弱酸盐,水解显碱性,故D不选;
故选:C.
点评 本题考查了盐类水解的性质和应用,明确明矾的成分及水解性质是解题关键,题目难度不大.

练习册系列答案
相关题目
12.在电解水制取H2和O2时,为了增强导电性,常常在水中加入一些电解质,下列物质可选用( )
| A. | NaCl | B. | CuCl2 | C. | NaOH | D. | CuSO4 |
10.某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液也不产生沉淀以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
| A. | 配合物中中心原子的电荷数和配位数均为6 | |
| B. | Pt4+提供孤对电子 | |
| C. | Cl-和NH3分子均与Pt4+配位 | |
| D. | 配合物中Cl-与Pt4+配位,而NH3分子不配位 |
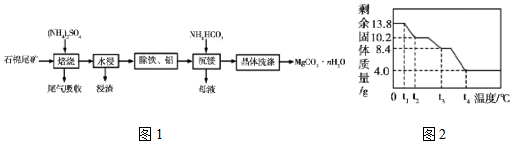
17.卤块主要成分是MgCl2,还含此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按如图所示流程进行生产,可制得轻质氧化镁.
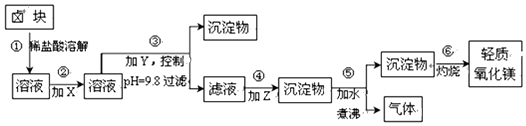
相关数据:
请根据表提供的资料回答:
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的a、c、d(选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)为尽量除去杂质,步骤③控制pH为9.8时,停止加入Y.调节为该pH的目的是使Mg2+以外的杂质尽可能彻底地转化为沉淀除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是ABCE.
A.酒精喷灯 B.铁三角架 C.坩埚 D.蒸发皿 E.泥三角 F.烧杯 G.石棉网
(5)已知在25℃时,Ksp[Mg(OH)2)=3.2×10-11,向0.02mol•L-1的MgCL2溶液中加入NaOH固体,如要生成Mg( OH )2沉淀,应使溶液中的c( OH-)最小为4×10-5 mol•L-1.
(6)为了分析制取的产品中残留铁元素的含量,取5g产品,先将Fe3+预处理为Fe2+后配制成100mL溶液,取25.00mL,用0.01mol•L-1KMnO4标准溶液在酸性条件下进行滴定.
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液的紫红色可指示反应终点.
②终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是4.480%.
(7)判断下列操作对测定结果的影响(填“偏高“、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的KMnO4溶液有少量溅出,使测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果偏低.

相关数据:
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6 | b.双氧水(含30%H2O2) | 1500 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2200 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO) | 800 |
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的a、c、d(选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)为尽量除去杂质,步骤③控制pH为9.8时,停止加入Y.调节为该pH的目的是使Mg2+以外的杂质尽可能彻底地转化为沉淀除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是ABCE.
A.酒精喷灯 B.铁三角架 C.坩埚 D.蒸发皿 E.泥三角 F.烧杯 G.石棉网
(5)已知在25℃时,Ksp[Mg(OH)2)=3.2×10-11,向0.02mol•L-1的MgCL2溶液中加入NaOH固体,如要生成Mg( OH )2沉淀,应使溶液中的c( OH-)最小为4×10-5 mol•L-1.
(6)为了分析制取的产品中残留铁元素的含量,取5g产品,先将Fe3+预处理为Fe2+后配制成100mL溶液,取25.00mL,用0.01mol•L-1KMnO4标准溶液在酸性条件下进行滴定.
①滴定前是否要滴加指示剂?否(填“是”或“否”),请说明理由KMnO4溶液的紫红色可指示反应终点.
②终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是4.480%.
(7)判断下列操作对测定结果的影响(填“偏高“、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的KMnO4溶液有少量溅出,使测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果偏低.
7. 甲酸香叶脂(结构如图)为无色透明液体,具有新鲜蔷薇嫩叶的香味,可用于配制香精.下列有关该有机物的叙述正确的是( )
甲酸香叶脂(结构如图)为无色透明液体,具有新鲜蔷薇嫩叶的香味,可用于配制香精.下列有关该有机物的叙述正确的是( )
 甲酸香叶脂(结构如图)为无色透明液体,具有新鲜蔷薇嫩叶的香味,可用于配制香精.下列有关该有机物的叙述正确的是( )
甲酸香叶脂(结构如图)为无色透明液体,具有新鲜蔷薇嫩叶的香味,可用于配制香精.下列有关该有机物的叙述正确的是( )| A. | 分子式为C11H18O2 | |
| B. | 含有羧基和碳碳双键两种官能团 | |
| C. | 能发生加成反应和水解反应 | |
| D. | 23gNa与过量的该物质反应生成标准状况下11.2L气体 |
11.下列有关说法正确的是( )
| A. | 加热坩埚中的硫酸铜晶体,失水后须在干燥器中冷却,再称量 | |
| B. | 检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热 | |
| C. | 用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 | |
| D. | 做锌铜稀硫酸原电池实验时,反应一段时间后锌片表面还是呈银白色 |
16.某混合气体可能含有N2、HCl、CO,依次进行如下处理,(假定每次处理均完全)( )
(1)通过足量的碳酸氢钠溶液和灼热的氧化铜,气体体积都没有变化;
(2)通过足量的过氧化钠固体,气体体积减小;
(3)通过灼热的铜网,经充分反应后气体体积又减小,但还剩余气体,由此可以确定原混合气体中.
(1)通过足量的碳酸氢钠溶液和灼热的氧化铜,气体体积都没有变化;
(2)通过足量的过氧化钠固体,气体体积减小;
(3)通过灼热的铜网,经充分反应后气体体积又减小,但还剩余气体,由此可以确定原混合气体中.
| A. | 一定没有N2,HCl 和CO中至少有一种 | |
| B. | 一定有N2,HCl 和CO | |
| C. | 一定有N2HCl 和CO中至少有一种 | |
| D. | 一定有N2 和HCl,没有CO |
 →
→ .
.