题目内容
5.在0.5L的密闭容器中,一定量的氮气与氢气进行如下反应:N2(g)+3H2(g)?2NH3(g)△H=a kJ•mol-1,其化学平衡常数K与温度的关系如下.| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,a小于(填“大于”、“小于”或“等于”)0.
(2)200℃时,向此密闭容器中充入0.20mol的N2和0.80mol的H2,反应初始6s内达到了平衡状态,N2的平均反应速率v(N2)=0.03mol•L-1•s-1.则6s时NH3的物质的量为0.18mol,c(N2)=0.22mol•L-1;此时N2的转化率为45%,如果这时向该密闭容器中再充入1mol氩气,N2的转化率不变(填“增大”“不变”“减小”).
(3)400℃时,2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,测得氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol时,该反应的v正(N2)大于(填“大于”、“小于”或“等于”)v逆(N2).
分析 (1)根据化学平衡常数概念写;由表中数据可知,随温度升高平衡常数减小,说明升高温度N2(g)+3H2(g)?2NH3(g)平衡逆向移动,则正反应为放热反应;
(2)根据氮气的反应速率计算6s内氮气的物质的量的变化,可得6s末氨气的物质的量,再根据转化率=$\frac{物质的转化量}{物质的起始量}$×100%计算;向该密闭容器中再充入1mol氩气,化学平衡不移动,转化率不变;
(3)400℃时,2NH3(g)?N2(g)+3H2(g)与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数关系;计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行.
解答 解:(1)反应N2(g)+3H2(g)?2NH3(g),K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$;由表中数据可知,随温度升高平衡常数减小,说明升高温度N2(g)+3H2(g)?2NH3(g平衡逆向移动,则正反应为放热反应,故a<0;
故答案为:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$;小于;
(2)在0.5L的密闭容器中,向此密闭容器中充入0.20mol的N2和0.80mol的H2,初始6s内达到了平衡状态,N2的平均反应速率v(N2)=0.03mol•L-1•s-1,则△c(N2)=0.03mol•L-1•s-1×6s=0.18mol•L-1,则6s时c(N2)=0.20mol÷0.5L-0.18mol•L-1=0.22mol•L-1;根据反应6s时NH3的物质的量为0.18mol•L-1×0.5L×
2=0.18mol;此时N2的转化率为$\frac{0.18mol•{L}^{-1}×0.5L}{0.2mol}$×100%=45%;该密闭容器中再充入1mol氩气,化学平衡不移动,则氮气的转化率不变;
故答案为:0.18;0.22;45%;不变;
(3)400℃时,2NH3(g)?N2(g)+3H2(g)与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数关系,故400℃时,2NH3(g)?N2(g)+3H2(g)的平衡常数为:$\frac{1}{0.5}$=2,氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol时,此时浓度商Qc=$\frac{(2÷0.5)×(1÷0.5)^{2}}{(3÷0.5)^{3}}$=0.89<K=2,反应向正反应进行,v正(N2)>v逆(N2);
故答案为:2;大于.
点评 本题考查化学平衡计算,涉及平衡常数及其应用,注意平衡常数只受温度影响,平衡常数及其单位与化学计量数有关,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
(1)工业上利用甲烷和氧气直接氧化制取甲醇的反应如下:
CH4+$\frac{1}{2}$O2(g)?CH3OH(g)△H=-128.5kJ/mol
副反应有:CH4(g)+$\frac{3}{2}$O2(g)?CO(g)+2H2O(g)△H=a kJ/mol
CH4(g)+2O2(g)?CO2(g)+2H2O(g)△H=b kJ/mol
CH4(g)+O2(g)?HCHO(g)+H2O(g)△H=c kJ/mol
甲醇与氧气反应生成HCHO(g)和水蒸汽的热化学方程式为CH3OH(g)+$\frac{1}{2}$O2(g)→HCHO(g)+H2O(g)△H=(c+128.5)KJ•L-1.
(2)苯乙烷(C8H10)生产苯乙烯(C8H8)的反应:C8H10(g)?C8H8(g)+H2(g)△H>0.T1℃下,将0.40mol苯乙烷充入2L密闭容器中反应,不同时间容器内n(C8H10)如表:
| 时间/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
②改变温度为T2℃,其他条件不变,测得平衡时容器内气体压强为反应前的1.4倍,则此时苯乙烷的转化率为40%.
(3)用惰性电极电解葡萄糖[CH2OH(CHOH)4CHO]和硫酸钠混合溶,可以制得葡萄糖酸[CH2OH(CHOH)4COOH]和己六醇[CH2OH(CHOH)4CH2OH].电解过程中,葡萄糖酸在阳极生成,对应的电极反应式CH2OH(CHOH)4CHO+H2O-2e-═CH2OH(CHOH)4COOH+2H+.
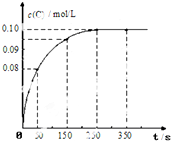 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )| A. | 反应在0~50s的平均速率v(C)=1.6×10-3mol/(L•s) | |
| B. | 该温度下,反应的平衡常数K=0.025 | |
| C. | 保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0 | |
| D. | 反应达平衡后,再向容器中充入 1 mol A,该温度下再达到平衡时0.1mol/L<c(C)<0.2mol/L |
 .
. 乙醇可用来制取乙醛、乙醚、乙酸乙酯等化工原料,也是制取染料、涂料、洗涤剂等产品的原料.
乙醇可用来制取乙醛、乙醚、乙酸乙酯等化工原料,也是制取染料、涂料、洗涤剂等产品的原料.