题目内容
(22分)如下图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液。
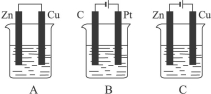
(1)A、B、C三个装置中属于原电池的是_____________。
(2)A池中Zn是_____________极, Cu极发生_____________反应,电极反应为_____________。反应过程溶液中c(Cu2+)_____________(填“变大”“变小”或“不变”)。
(3)B池中C棒发生_________反应,电极反应为_________。B 池中的总反应为_ __。
(4)C池中Zn极的反应现象为 _____________。Cu极电极反应为_____________。反应过程溶液中c(Cu2+)_____________(填“变大”“变小”或“不变”)。
(1)A(2)负 还原反应 Cu2++ 2e-=Cu 变小(3)Cu2++ 2e-=Cu CuCl2  Cu+ Cl2↑ (4)有红色物质生成 Cu – 2e-=Cu2+ 不变
Cu+ Cl2↑ (4)有红色物质生成 Cu – 2e-=Cu2+ 不变
【解析】
试题分析:(1)B、C两个装置有外接电源,是电解池,A是原电池。(2)Zn比较活泼,在原电池中做负极,Cu做正极,正极发生还原反应,Cu2+在正极得到电子变成Cu,电极反应为:Cu2++ 2e-=Cu,Cu2+发生了反应,则c(Cu2+)变小。(3)B池中C接电源的负极,做阴极,阳离子在阳极放电,电极反应为Cu2++ 2e-=Cu,总反应为:CuCl2  Cu+ Cl2↑(4)C池中Zn极做阴极,Cu2+放电变为Cu,所以可以看到有红色物质生成,Cu极做阳极,Cu是活性材料,所以阳极是Cu放电,电极反应为:Cu – 2e-=Cu2+,阴极消耗Cu2+,阳极生成Cu2+,所以溶液中c(Cu2+)不变。
Cu+ Cl2↑(4)C池中Zn极做阴极,Cu2+放电变为Cu,所以可以看到有红色物质生成,Cu极做阳极,Cu是活性材料,所以阳极是Cu放电,电极反应为:Cu – 2e-=Cu2+,阴极消耗Cu2+,阳极生成Cu2+,所以溶液中c(Cu2+)不变。
考点:原电池和电解池的两极判断,电极反应方程式的书写以及实验现象的描述。

 Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将
Fe(SCN)3 +3KCl。已知Fe(SCN)3呈红色,则在该平衡体系中加入少量KCl晶体后(忽略溶液体积的变化),红色将