题目内容
碳酸氢铵是一种重要的铵盐.实验室中,将二氧化碳通入氨水可制得碳酸氢铵,用碳酸氢铵和氯化钠可制得纯碱.
完成下列填空:
(1)二氧化碳通入氨水的过程中,先有 晶体(填写化学式)析出,然后晶体溶解,最后析出NH4HCO3晶体.
(2)含0.800mol NH3的水溶液质量为54.0g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为 %.
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠.实验步骤依次为:
①粗盐溶解;
②加入试剂至沉淀完全,煮沸;
③ ;
④加入盐酸调pH;
⑤加入 ;
⑥过滤;
⑦灼烧,冷却,称重.
(4)上述步骤②中所加入的试剂为 、 .
(5)上述步骤④中加盐酸调pH的目的是 .
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:
含0.1mol NH4HCO3的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液.
若有沉淀,则NH4HCO3与NaOH的反应可能为 (写离子方程式);
若无沉淀,则NH4HCO3与NaOH的反应可能为 (写离子方程式).
该实验方案有无不妥之处?若有,提出修正意见 .
完成下列填空:
(1)二氧化碳通入氨水的过程中,先有
(2)含0.800mol NH3的水溶液质量为54.0g,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.2g,则NH4HCO3的产率为
(3)粗盐(含Ca2+、Mg2+)经提纯后,加入碳酸氢铵可制得碳酸钠.实验步骤依次为:
①粗盐溶解;
②加入试剂至沉淀完全,煮沸;
③
④加入盐酸调pH;
⑤加入
⑥过滤;
⑦灼烧,冷却,称重.
(4)上述步骤②中所加入的试剂为
(5)上述步骤④中加盐酸调pH的目的是
(6)为探究NH4HCO3和NaOH的反应,设计实验方案如下:
含0.1mol NH4HCO3的溶液中加入0.1mol NaOH,反应完全后,滴加氯化钙稀溶液.
若有沉淀,则NH4HCO3与NaOH的反应可能为
若无沉淀,则NH4HCO3与NaOH的反应可能为
该实验方案有无不妥之处?若有,提出修正意见
考点:物质分离、提纯的实验方案设计
专题:
分析:(1)二氧化碳和一水合氨发生的反应为CO2+2NH3.H2O=(NH4)2CO3、(NH4)2CO3+CO2+H2O=2NH4HCO3;
(2)根据碳原子守恒计算理论上m(NH4HCO3),根据题意计算实际m(NH4HCO3),从而计算其产率;
(3)粗盐提纯操作步骤为:溶解、加入沉淀剂、过滤,然后向滤液中加入稀盐酸,调节溶液的pH,再向溶液中加入碳酸氢铵,即可得到溶解度较小的NaHCO3,再过滤、洗涤得到较纯净的NaHCO3,最后加热NaHCO3得到Na2CO3;
(4)用NaOH除去OH-,用Na2CO3除去Ca 2+;
(5)除去过量的NaOH、Na2CO3;
(6)若有沉淀,说明溶液中含有CO32-,则HCO3-和 OH-反应生成CO32-,如果没有沉淀,说明溶液中不存在CO32-,则NH4+和OH-发生反应.
(2)根据碳原子守恒计算理论上m(NH4HCO3),根据题意计算实际m(NH4HCO3),从而计算其产率;
(3)粗盐提纯操作步骤为:溶解、加入沉淀剂、过滤,然后向滤液中加入稀盐酸,调节溶液的pH,再向溶液中加入碳酸氢铵,即可得到溶解度较小的NaHCO3,再过滤、洗涤得到较纯净的NaHCO3,最后加热NaHCO3得到Na2CO3;
(4)用NaOH除去OH-,用Na2CO3除去Ca 2+;
(5)除去过量的NaOH、Na2CO3;
(6)若有沉淀,说明溶液中含有CO32-,则HCO3-和 OH-反应生成CO32-,如果没有沉淀,说明溶液中不存在CO32-,则NH4+和OH-发生反应.
解答:
解:(1)将CO2通入氨水中首先生成(NH4)2CO3晶体析出,随CO2不断通入,(NH4)2CO3和CO2作用转化为NH4HCO3晶体,最终析出NH4HCO3晶体,发生的反应为CO2+2NH3.H2O=(NH4)2CO3+H2O、(NH4)2CO3+CO2+H2O=2NH4HCO3,总反应式为CO2+NH3?H2O=NH4HCO3,
故答案为:(NH4)2CO3;
(2)该氨水完全反应需通入0.8molCO2,过滤得到m(NH4HCO3)=54.0g+0.8mol×44g?mol-1-31.2g=58g,根据碳原子守恒,理论上应得到m(NH4HCO3)=0.8mol×79g?mol-1=63.2g,则NH4HCO3的产率为
×100%=92%,故答案为:92%;
(3)粗盐提纯步骤应是向粗盐溶液中加入沉淀剂、过滤(除去沉淀),然后加入盐酸,调pH(除去前面加入沉淀剂引入的OH-与CO32-),此时溶液为纯净的NaCl溶液,再向该溶液中加入NH4HCO3,即可析出溶解度较小的NaHCO3,然后过滤、洗涤得到纯净NaHCO3,将NaHCO3加热得到Na2CO3,
故答案为:过滤;NH4HCO3;
(4)步骤2中加入沉淀剂为NaOH(用来除去Mg2+)、碳酸钠(用来除去Ca2+),发生的反应分别为 2OH-+Mg2+=Mg(OH)2↓、CO32-+Ca2+=CaCO3↓,
故答案为:NaOH;Na2CO3;
(5)步骤④中加盐酸调pH的目的是除去过量的NaOH、Na2CO3,故答案为:除去过量的NaOH、Na2CO3;
(6)因向NH4HCO3溶液中加入NaOH时,发生的离子反应有:HCO3-+OH-=CO32-+H2O与NH4++OH-=NH3?H2O,若NaOH量不足,则两反应存在先后次序问题,故实验中若产生沉淀,说明反应后溶液中含有CO32-,证明先发生HCO3-+OH-=CO32-+H2O,否则先发生NH4++OH-=NH3?H2O,如果不煮沸,产生的NH3.H2O不会分解而逸出氨气,在Ca 2+存在的条件下,溶液中NH3.H2O能够将HCO3-变成CO32-,所以也会有CaCO3沉淀生成,最终与前一种现象相同,先煮沸,就是为了驱除溶液中的NH3,如果NH3不存在,则HCO3-不能与Ca 2+反应,进而将两种现象区分开,
故答案为:HCO3-+OH-=CO32-+H2O;NH4++OH-=NH3?H2O;需先煮沸,然后滴加氯化钙稀溶液.
故答案为:(NH4)2CO3;
(2)该氨水完全反应需通入0.8molCO2,过滤得到m(NH4HCO3)=54.0g+0.8mol×44g?mol-1-31.2g=58g,根据碳原子守恒,理论上应得到m(NH4HCO3)=0.8mol×79g?mol-1=63.2g,则NH4HCO3的产率为
| 58g |
| 63.2g |
(3)粗盐提纯步骤应是向粗盐溶液中加入沉淀剂、过滤(除去沉淀),然后加入盐酸,调pH(除去前面加入沉淀剂引入的OH-与CO32-),此时溶液为纯净的NaCl溶液,再向该溶液中加入NH4HCO3,即可析出溶解度较小的NaHCO3,然后过滤、洗涤得到纯净NaHCO3,将NaHCO3加热得到Na2CO3,
故答案为:过滤;NH4HCO3;
(4)步骤2中加入沉淀剂为NaOH(用来除去Mg2+)、碳酸钠(用来除去Ca2+),发生的反应分别为 2OH-+Mg2+=Mg(OH)2↓、CO32-+Ca2+=CaCO3↓,
故答案为:NaOH;Na2CO3;
(5)步骤④中加盐酸调pH的目的是除去过量的NaOH、Na2CO3,故答案为:除去过量的NaOH、Na2CO3;
(6)因向NH4HCO3溶液中加入NaOH时,发生的离子反应有:HCO3-+OH-=CO32-+H2O与NH4++OH-=NH3?H2O,若NaOH量不足,则两反应存在先后次序问题,故实验中若产生沉淀,说明反应后溶液中含有CO32-,证明先发生HCO3-+OH-=CO32-+H2O,否则先发生NH4++OH-=NH3?H2O,如果不煮沸,产生的NH3.H2O不会分解而逸出氨气,在Ca 2+存在的条件下,溶液中NH3.H2O能够将HCO3-变成CO32-,所以也会有CaCO3沉淀生成,最终与前一种现象相同,先煮沸,就是为了驱除溶液中的NH3,如果NH3不存在,则HCO3-不能与Ca 2+反应,进而将两种现象区分开,
故答案为:HCO3-+OH-=CO32-+H2O;NH4++OH-=NH3?H2O;需先煮沸,然后滴加氯化钙稀溶液.
点评:本题考查了物质的分离和检验,明确物质性质及实验基本操作是解本题关键,同时考查学生分析问题、解决问题能力,明确反应原理,根据物质的性质分析解答,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
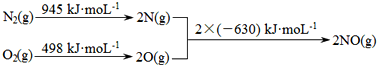
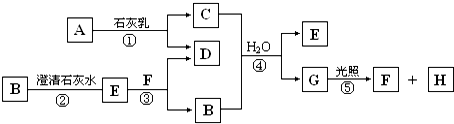
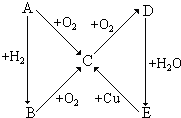 根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质的化学式和有关反应的化学方程式.
根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质的化学式和有关反应的化学方程式.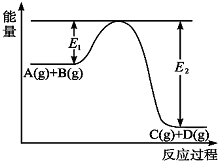 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.