题目内容
6.X、Y、Z是短周期的三种相邻元素,X与Y同主族,Y与Z同周期,已知三种元素族序数之和为16,原子序数之和为38,则X、Y、Z的元素符号为( )| A. | Na、K、Ca | B. | N、P、S | C. | F、Cl、S | D. | O、S、Cl |
分析 X、Y、Z是周期表中相邻的三种短周期元素,X与Y同主族,Y与Z同周期,三种元素族序数之和为16,设Z元素的最外层电子数为x,则X、Y最外层电子数为x+1或x-1,若X、Y元素的最外层电子数为x+1,则x+2(x+1)=16,解得x=$\frac{14}{3}$,不符合题意;若X、Y元素的最外层电子数为x-1,则有x+2(x-1)=16,解得x=6,即XY位于第VA族,Z位于第VIA族,原子序数之和为38,Z的原子序数为38-7-15=16,结合原子序数之和判断,据此解答.
解答 解:X、Y、Z是周期表中相邻的三种短周期元素,X与Y同主族,Y与Z同周期,三种元素族序数之和为16,设Z元素的最外层电子数为x,则X、Y最外层电子数为x+1或x-1,若X、Y元素的最外层电子数为x+1,则x+2(x+1)=16,解得x=$\frac{14}{3}$,不符合题意;若X、Y元素的最外层电子数为x-1,则有x+2(x-1)=16,解得x=6,即XY位于第VA族,Z位于第VIA族,原子序数之和为38,Z的原子序数为38-7-15=16,则Z为S元素,故X为N元素、Y为P元素;
故选B.
点评 本题考查原子结构与位置关系,难度中等,关键是根据最外层电子数之和为16确定元素所在主族,注意掌握短周期元素的特点,也可以利用验证法进行判断,侧重于考查学生的分析能力.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
16.反应2SO2+O2?2SO3达到平衡后,再向反应器中充入由18O组成的氧气,经一段时间后,18O可能存在于( )
| A. | 生成的SO3中 | B. | O2和SO3中 | C. | 剩余的SO3中 | D. | O2、SO2和SO3中 |
17.下列物质之间的相互关系不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | O2和O3互为同素异形体 | ||
| C. | H、D、T互为同位素 | D. | 干冰和冰为同一种物质 |
1.下列各组固体混合物中,能用过滤的操作方法进行分离的是( )
| A. | NaCl和KNO3 | B. | BaCO3和MnO2 | C. | CaCO3和Na2CO3 | D. | KOH和NaNO3 |
11.有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示:
下列各项判断正确的是( )
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se 42.0 | H2Te-1.8 |
| A. | 第一组和第二组物质中一定含有共价键 | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr>H2Se | |
| C. | 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强 |
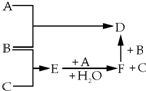 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.
有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.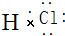 ;
;