题目内容
最常见的塑化剂邻苯二甲酸二丁酯可由邻苯二甲酸酐与正丁醇在浓硫酸共热下反应制得,反应的化学方程式及装置图(部分装置省略)如下:
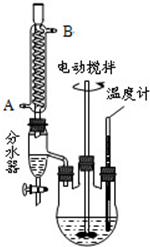
已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解.
邻苯二甲酸酐、正丁醇、邻苯二甲酸二酯实验操作流程如下:
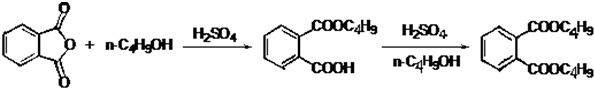
①向三颈烧瓶内加入30g 邻苯二甲酸酐16g 正丁醇以及少量浓硫酸.
②搅拌,升温至105℃,持续搅拌反应2小时.升温至140℃,搅拌、保温至反应结束.
③冷却至室温,将反应混合物倒出.通过工艺流程中的操作X,得到粗产品.
④粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏
请回答以下问题:
(1)邻苯二甲酸酐和正丁醇反应时加入浓硫酸的作用是 .
(2)步骤②中不断从分水器下部分离出产物水的目的是 .判断反应已结束的方法是 .
(3)反应的第一步进行得迅速而完全.第二步是可逆反应,进行较缓慢,为使反应向生成邻苯二甲酸二丁酯的方向进行,可采取的措施是: .
A.增大压强 B.增加正丁醇的量 C.分离出水 D.增加催化剂用量
(4)操作X中,应先用5% Na2CO3溶液洗涤粗产品.纯碱溶液浓度不宜过高,更不能使用氢氧化钠.若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示): .
(5)粗产品提纯流程中采用减压蒸馏的目的是 .
(6)用测定相对分子质量的方法,可以检验所得产物是否纯净.现代分析方法中测定有机物相对分子质量通常采用的是 .

已知:正丁醇沸点118℃,纯邻苯二甲酸二丁酯是无色透明、具有芳香气味的油状液体,沸点340℃,酸性条件下,温度超过180℃时易发生分解.
邻苯二甲酸酐、正丁醇、邻苯二甲酸二酯实验操作流程如下:

①向三颈烧瓶内加入30g 邻苯二甲酸酐16g 正丁醇以及少量浓硫酸.
②搅拌,升温至105℃,持续搅拌反应2小时.升温至140℃,搅拌、保温至反应结束.
③冷却至室温,将反应混合物倒出.通过工艺流程中的操作X,得到粗产品.
④粗产品用无水硫酸镁处理至澄清→取清液(粗酯)→圆底烧瓶→减压蒸馏
请回答以下问题:
(1)邻苯二甲酸酐和正丁醇反应时加入浓硫酸的作用是
(2)步骤②中不断从分水器下部分离出产物水的目的是
(3)反应的第一步进行得迅速而完全.第二步是可逆反应,进行较缓慢,为使反应向生成邻苯二甲酸二丁酯的方向进行,可采取的措施是:
A.增大压强 B.增加正丁醇的量 C.分离出水 D.增加催化剂用量
(4)操作X中,应先用5% Na2CO3溶液洗涤粗产品.纯碱溶液浓度不宜过高,更不能使用氢氧化钠.若使用氢氧化钠溶液,对产物有什么影响?(用化学方程式表示):
(5)粗产品提纯流程中采用减压蒸馏的目的是
(6)用测定相对分子质量的方法,可以检验所得产物是否纯净.现代分析方法中测定有机物相对分子质量通常采用的是
考点:制备实验方案的设计
专题:实验题
分析:(1)浓硫酸在反应中起到催化作用,加快反应速率;
(2)水是生成物,不断的分离生成物,使平衡向着正向移动,可以提高反应物的转化率;反应结束时,反应体系的压强不再变化,分水器中的水位高度不变;
(3)根化学平衡及其影响进行分析;
(4)洗涤后的混合液体溶液会分层,通过分液漏斗进行分液分离;
(5)根据“沸点340℃,温度超过180℃时易发生分解”进行分析;
(6)现代分析方法中测定有机物相对分子质量通常采用的是质谱仪.
(2)水是生成物,不断的分离生成物,使平衡向着正向移动,可以提高反应物的转化率;反应结束时,反应体系的压强不再变化,分水器中的水位高度不变;
(3)根化学平衡及其影响进行分析;
(4)洗涤后的混合液体溶液会分层,通过分液漏斗进行分液分离;
(5)根据“沸点340℃,温度超过180℃时易发生分解”进行分析;
(6)现代分析方法中测定有机物相对分子质量通常采用的是质谱仪.
解答:
解:(1)在反应中,浓硫酸起到了催化作用,加快了反应速率,
故答案为:催化剂;
(2)不断的分离出生成物水,可以使反应向着正向移动,提高了反应物产率;由于反应结束时,反应体系的压强不再变化,分水器中的水位高度不变,
故答案为:使用分水器分离出水,有利于反应平衡向生成邻苯二甲酸二丁酯的方向移动,提高产率;分水器中的水位高度保持基本不变时;
(3)A.增大压强:该反应中没有气体参加,压强不影响化学平衡,最大压强,平衡不发生移动,故A错误;
B.增加正丁醇的量:反应物浓度增大,可以使平衡向着生成邻苯二甲酸二丁酯的方向移动,故B正确;
C.分离出水:减小了生成物浓度,则平衡向着生成邻苯二甲酸二丁酯的方向移动,故C正确;
D.增加催化剂用量,催化剂影响反应速率,不影响化学平衡,故D错误;
故答案为:BC;
(4)若使用氢氧化钠溶液,会发生反应: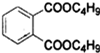 +2NaOH→
+2NaOH→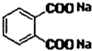 +2C4H9OH,得不到产物邻苯二甲酸二丁酯,
+2C4H9OH,得不到产物邻苯二甲酸二丁酯,
故答案为: +2NaOH→
+2NaOH→ +2C4H9OH;
+2C4H9OH;
(5)由于邻苯二甲酸二丁酯沸点340℃,温度超过180℃时易发生分解,减压可使其沸点降低,
故答案为:邻苯二甲酸二甲酯沸点较高,高温会造成其分解,减压可使其沸点降低;
(6)现代分析方法中测定有机物相对分子质量通常采用的是质谱仪,
故答案为:质谱仪.
故答案为:催化剂;
(2)不断的分离出生成物水,可以使反应向着正向移动,提高了反应物产率;由于反应结束时,反应体系的压强不再变化,分水器中的水位高度不变,
故答案为:使用分水器分离出水,有利于反应平衡向生成邻苯二甲酸二丁酯的方向移动,提高产率;分水器中的水位高度保持基本不变时;
(3)A.增大压强:该反应中没有气体参加,压强不影响化学平衡,最大压强,平衡不发生移动,故A错误;
B.增加正丁醇的量:反应物浓度增大,可以使平衡向着生成邻苯二甲酸二丁酯的方向移动,故B正确;
C.分离出水:减小了生成物浓度,则平衡向着生成邻苯二甲酸二丁酯的方向移动,故C正确;
D.增加催化剂用量,催化剂影响反应速率,不影响化学平衡,故D错误;
故答案为:BC;
(4)若使用氢氧化钠溶液,会发生反应:
 +2NaOH→
+2NaOH→ +2C4H9OH,得不到产物邻苯二甲酸二丁酯,
+2C4H9OH,得不到产物邻苯二甲酸二丁酯,故答案为:
 +2NaOH→
+2NaOH→ +2C4H9OH;
+2C4H9OH;(5)由于邻苯二甲酸二丁酯沸点340℃,温度超过180℃时易发生分解,减压可使其沸点降低,
故答案为:邻苯二甲酸二甲酯沸点较高,高温会造成其分解,减压可使其沸点降低;
(6)现代分析方法中测定有机物相对分子质量通常采用的是质谱仪,
故答案为:质谱仪.
点评:本题通过制备邻苯二甲酸二丁酯的实验,考查了物质制备方案的设计方法,试题设计的知识点较多、综合性较强,充分考查的学生的分析、理解能力及化学实验能力,正确分析制备原理为解答关键.

练习册系列答案
相关题目
某溶液中可能含有以下6种离子中的几种:NH4+、A13+、Mg2+、CO32-、Cl-、SO42-,为确认溶液的组成,现取100mL分成三等份溶液进行如下实验:
(1)向第一份溶液中加入 AgNO3溶液有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液充分反应后,最终得到沉淀0.58g,同时收集到气体0.03mol(设气体全部从溶液中逸出);
(3)向第三份溶液中加入足量BaCl2溶液(盐酸酸化)充分反应后,得到沉淀6.99g.
由此可知,下列关于原溶液组成的正确结论是( )
(1)向第一份溶液中加入 AgNO3溶液有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液充分反应后,最终得到沉淀0.58g,同时收集到气体0.03mol(设气体全部从溶液中逸出);
(3)向第三份溶液中加入足量BaCl2溶液(盐酸酸化)充分反应后,得到沉淀6.99g.
由此可知,下列关于原溶液组成的正确结论是( )
| A、溶液中SO42-的浓度是0.3 mol/L |
| B、溶液中一定含有A13+和NH4+ |
| C、一定不存在Mg2+,可能存在A13+ |
| D、一定存在Cl- 可能含CO32- |
与乙炔具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是( )
| A、丙炔 | B、环丁烷 | C、甲苯 | D、苯 |
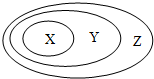 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )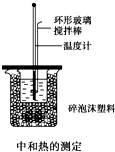 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题: