题目内容
10.下列关于物质应用的说法错误的是( )| A. | 玻璃容器可长期盛放各种酸 | |
| B. | 水中加入明矾、硫酸铁溶液可以起净水作用 | |
| C. | Al2O3可制造耐高温的实验仪器 | |
| D. | Na2S可除去污水中有毒的Cu2+ |
分析 A.氢氟酸能够与二氧化硅反应;
B.依据盐类水解的性质解答;
C.耐高温材料应具有较高的熔点;
D.Na2S可以和Cu2+发生反应.
解答 解:A.玻璃中含有二氧化硅,氢氟酸能够与二氧化硅反应,腐蚀玻璃,所以不能用玻璃容器盛放氢氟酸,故A错误;
B.水中加入明矾、硫酸铁溶液,铝离子、铁离子水解生成的氢氧化铝胶体、氢氧化铁胶体具有吸附性,所以可以起净水作用,故B正确;
C.Al2O3熔点高,制造耐高温的实验仪器,故C正确;
D.Na2S中的硫离子可以和Cu2+发生反应生成硫化铜沉淀,Na2S可除去污水中的Cu2+,故D正确;
故选:A.
点评 本题考查学生物质的性质以及应用方面的知识,熟悉相关物质的性质是解题关键,注意知识的归纳和梳理是关键,难度不大.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案
相关题目
1.下列化学式既能表示物质的组成,又能表示物质的一个分子的是( )
| A. | NH3 | B. | NaOH | C. | SiO2 | D. | Fe |
5.下列反应的离子方程式正确的是( )
| A. | 铁和稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙溶于稀盐酸中 CO32-+2H+═CO2+H2O | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 碳酸氢钠溶液与盐酸反应 HCO3-+H+═CO2↑+H2O |
15.分类方法在化学学科的发展中起着非常重要的作用.下列分类标准合理的是( )
| A. | 根据物质能否导电将物质分为电解质和非电解质 | |
| B. | 根据反应中的热效应将化学反应分为放热反应和吸热反应 | |
| C. | 根据溶液导电性强弱将电解质分为强电解质和弱非电解质 | |
| D. | 根据元素的化合价的高低将化学反应分为氧化还原反应和非氧化还原反应 |
3.下列描述中,错误的是( )
| A. | 电解MgCl2饱和溶液,可制得Cl2,但得不到镁 | |
| B. | 镁与稀盐酸反应剧烈,加入碳酸钠晶体可以减慢反应速率 | |
| C. | 电解饱和食盐水制氯气时用铁作阳极 | |
| D. | 电解法精炼粗铜,用纯铜作阴极 |
1.甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料.
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H
?下表所列数据是该反应在不同温度下的化学平衡常数(K).
由表中数据判断反应I为放热反应(填“吸”或“放”).
?某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃(从表中选择).
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1 kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2 kJ/mol
③H2O(g)=H2O(l)△H3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=(△H1-△H2+4△H3)/2kJ/mol(用△H1、△H2、△H3表示)
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72?)时,实验室利用如图装置模拟该法:
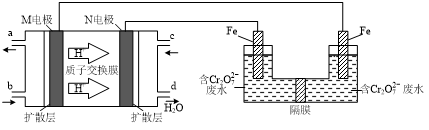
①N电极的电极反应式为O2+4e?+4H+=2H2O.
②请完成电解池中Cr2O72?转化为Cr3+的离子反应方程式:
Cr2O72?+6Fe2++14H+═2Cr3++6Fe3++7H2O
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10?5mol•L-1 时,Cr3+沉淀完全,此时溶液的pH=5.6. (已知,Ksp=6.4×10?31,lg2=0.3)
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H
?下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
?某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃(从表中选择).
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1 kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2 kJ/mol
③H2O(g)=H2O(l)△H3 kJ/mol
则反应 CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=(△H1-△H2+4△H3)/2kJ/mol(用△H1、△H2、△H3表示)
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72?)时,实验室利用如图装置模拟该法:

①N电极的电极反应式为O2+4e?+4H+=2H2O.
②请完成电解池中Cr2O72?转化为Cr3+的离子反应方程式:
Cr2O72?+6Fe2++14H+═2Cr3++6Fe3++7H2O
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10?5mol•L-1 时,Cr3+沉淀完全,此时溶液的pH=5.6. (已知,Ksp=6.4×10?31,lg2=0.3)
