题目内容
7.已知铬的原子序数为24,下列叙述不正确的是( )| A. | 铬位于元素周期表的第四周期第ⅥB族 | |
| B. | 已知铬元素的一种同位素的质量数为53,则该同位素有29个中子 | |
| C. | 中子数为29的铬原子符号表示为${\;}_{24}^{29}$Cr | |
| D. | 警察通过装有橙色酸性重铬酸钾溶液的装置检查司机是否酒后驾车 |
分析 铬的原子序数为24,第三周期稀有气体的原子序数为18,则Cr位于第四周期第ⅣB族,结合质子数+中子数=质量数及氧化还原反应来解答.
解答 解:A.铬的原子序数为24,于元素周期表的第四周期第ⅥB族,故A正确;
B.铬元素的一种同位素的质量数为53,则该同位素有53-24=29个中子,故B正确;
C.中子数为29的铬原子,其质量数为53,则原子符号表示为${\;}_{24}^{53}$Cr,故C错误;
D.橙色的酸性重铬酸钾具有强氧化性,与乙醇发生氧化还原反应,橙色变为黄色,以此可检查司机是否酒后驾车,故D正确;
故选C.
点评 本题考查较综合,涉及元素周期表的结构及应用、原子的构成及氧化还原反应等,为高频考点,把握原子序数确定元素的位置、性质为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
17.生活中处处有化学,下列有关说法正确的是( )
| A. | 饮用矿泉水瓶的主要成分是聚氯乙烯 | |
| B. | 淀粉和纤维素均为天然高分子化合物 | |
| C. | 凡含有食品添加剂的食物均不可食用 | |
| D. | 大米煮成粥后,淀粉就变成了葡萄糖 |
18.类推是中学化学中重要的思维方法.下列类推结论正确的是( )
| A. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 铝和硫加热得到Al2S3,故铁和硫加热得到Fe2S3 | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
2.若烷烃CH3CH2CH(CH3)CH(CH3)CH2CH3是烯烃与氢气的加成产物,烯烃可能的结构有a种,若该烷烃是炔烃与氢气的加成产物,炔烃可能的结构有b种,则a、b分别等于( )
| A. | 7、2 | B. | 7、1 | C. | 4、2 | D. | 4、1 |
12.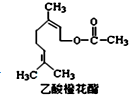 乙酸橙花酯是一种无色至微黄色油状液体,有橙花和玫瑰样香气,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
乙酸橙花酯是一种无色至微黄色油状液体,有橙花和玫瑰样香气,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
 乙酸橙花酯是一种无色至微黄色油状液体,有橙花和玫瑰样香气,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
乙酸橙花酯是一种无色至微黄色油状液体,有橙花和玫瑰样香气,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )| A. | 它的同分异构体中可能有芳香族化合物 | |
| B. | 能发生加成反应,但不能发生取代反应 | |
| C. | lmol该有机物在一定条件下和H2反应,共消耗H2为3mol | |
| D. | lmol该有机物水解时只能消耗lmo1NaOH |
19.某有机物1.8g在氧气中完全燃烧,只生成2.64g CO2和1.08H2O,下列说法正确的是( )
| A. | 该有机物仅含有碳、氢两种元素 | |
| B. | 该有机物中碳、氢原子的个数比是1:1 | |
| C. | 该有机物中一定含有氧元素 | |
| D. | 可以确定出该有机物的分子式 |
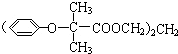 ,可用于降低血液中的胆固醇,该物质合成线路如图所示:
,可用于降低血液中的胆固醇,该物质合成线路如图所示: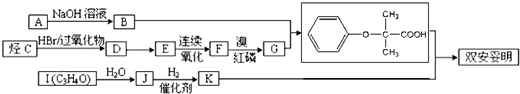
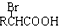 $\stackrel{苯酸钠}{→}$
$\stackrel{苯酸钠}{→}$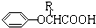
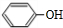 .
.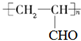
 +K→双安妥明”的化学方程式为
+K→双安妥明”的化学方程式为 .
.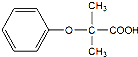 的同分异构体有6种(不考虑立体异构)
的同分异构体有6种(不考虑立体异构)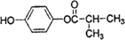 (写结构简式).
(写结构简式).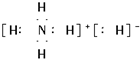 .
. .
.