题目内容
9.C60分子结构与足球形状相似,它与金刚石互为( )| A. | 同位素 | B. | 同分异构体 | C. | 同素异形体 | D. | 同种物质 |
分析 C60是一种只有碳元素组成的单质,金刚石也是只有碳元素组成的单质,且属于不同的单质,则二者互为同素异形体.
解答 解:A、同位素的分析对象是原子,而C60与金刚石属于单质,故A错误;
B、同分异构体的分析对象是化合物,而C60与金刚石属于单质,故B错误;
C、C60与金刚石是同种元素的不同单质,互为同素异形体,故C正确;
D、C60与足球有很相似的结构,金刚石是空间网状结构,结构不同,则不是同一种物质,故D错误;
故选C.
点评 本题考查基本概念,明确同位素、同素异形体、同分异构体的概念及概念中的要点是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.下列反应的生成物为纯净物的是( )
| A. | CH4和Cl2光照 | B. | 甲苯与液溴发生取代反应 | ||
| C. | CH2=CH-CH3与HCl加成产物 | D. | 乙烯和氯化氢加成 |
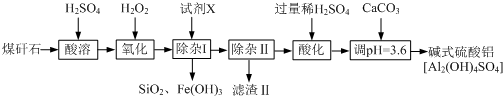
17.CoCl2•6H20是一种陶瓷着色剂.利用水钴矿[主要成分为Co203、Co(OH)3,还含少量Fe203、Al203、MnO等]制取CoCl2•6H20的工艺流程如图1:

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表:(金属离子浓度为:0.01mol/L)
③CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co(OH)3发生反应的离子方程式2Co(OH)3+SO32-+4H+=2Co2++SO42-+5H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)“加Na2CO3调pH至a”,则a的范围是5.2≤PH<7.6.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解;
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0〜2.5 B.3.0〜3.5 C.4.0〜4.5 D.5.0〜5.5
(6)操作1为蒸发浓缩、冷却结晶、过滤.
(7)实验室用足量的浓盐酸完全溶解一定量的钴的氧化物Cox0y(其中钴的化合价为+2、+3),若得到含13gCoCl2的溶液并产生标准状况下448mL的黄绿色气体,则y:x=6:5.

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co(OH)3发生反应的离子方程式2Co(OH)3+SO32-+4H+=2Co2++SO42-+5H2O.
(2)写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)“加Na2CO3调pH至a”,则a的范围是5.2≤PH<7.6.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解;
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是除去溶液中的Mn2+;其使用的最佳pH范围是B.
A.2.0〜2.5 B.3.0〜3.5 C.4.0〜4.5 D.5.0〜5.5
(6)操作1为蒸发浓缩、冷却结晶、过滤.
(7)实验室用足量的浓盐酸完全溶解一定量的钴的氧化物Cox0y(其中钴的化合价为+2、+3),若得到含13gCoCl2的溶液并产生标准状况下448mL的黄绿色气体,则y:x=6:5.
4.工业上常采用生物硝化法将NH4+转化NO3-的方法处理氨氮废水,工作流程如下,下列说法错误的是( )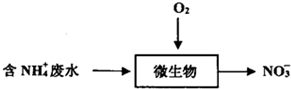

| A. | 生物硝化法处理废水,会导致水体pH逐渐下降:NH4++202=NO3-+2H++H20 | |
| B. | 长期过量使用NH4Cl等铵态化肥,易导致土壤酸化,水体富营养化 | |
| C. | 检验NH4+所需的试剂是浓NaOH溶液,湿润的蓝色石蕊试纸 | |
| D. | 微生物保持活性的pH范围为7〜9,可以加入石灰石来调节水体的pH |
14.NA为阿伏加罗常数的值,下列叙述正确的是( )
| A. | 1molCH3+中含有的电子数为10NA | |
| B. | 1mol铁粉与1mol水蒸气充分反应转移的电子数为3A | |
| C. | 0.1mol/L的Al2(SO4)3溶液中,Al3+的数目小于0.2NA | |
| D. | 电解精炼铜时,若转移了NA个电子,则阴极析出32g铜 |
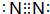 ,Z的原子结构示意图
,Z的原子结构示意图 .
.
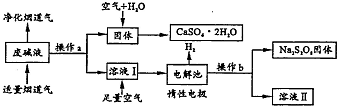
 为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下:
为了充分应用资源,用工业废碱液(Ca(OH)2、NaOH)与烟道气(回收成份SO2)来制取石膏(CaSO4•2H2O)和过二硫酸钠(Na2S2O8).设计简要流程如下: