题目内容
若
X表示X元素的一个原子,则该原子的( )
58 28 |
| A、核电荷数为30 |
| B、相对原子质量为58 |
| C、核内有30个中子 |
| D、核外有58个电子 |
考点:质子数、中子数、核外电子数及其相互联系
专题:
分析:原子符号AZX,左上角A为质量数,左下角Z为质子数,X代表元素符号,并且质量数=质子数+中子数,质子数=核电荷数=核外电子数.据此解答.
解答:
解:A.
X中核电荷数为28,故A错误;
B.
X中质量数为58,近似相对原子质量等于质量数为58,故B错误;
C.
X中质量数为58,质子数为28,则中子数=58-28=30,故C正确;
D.
X中质子数为28,质子数=核外电子数=28,故D错误;
故选C.
58 28 |
B.
58 28 |
C.
58 28 |
D.
58 28 |
故选C.
点评:本题考查学生对原子符号AZX理解,难度较小,关键明白原子符号的意义以及质量数=质子数+中子数.

练习册系列答案
相关题目
21世纪以来,国与国之间因对海权的争夺引起的摩擦不断,在捍卫主权的同时,人们看重的是海洋这个巨大资源的宝藏,下列有关海洋资源综合利用的说法不正确的是( )
| A、利用海水波浪发电是将动能转化为电能 |
| B、从海水中提取溴单质一定伴有化学变化 |
| C、海水中的铀元素以UCl4的形式存在,利用螯合型离子交换树脂可得到铀单质 |
| D、积极研发海水直接冷却技术,可减少煤炭的使用量,有利于环境保护 |
现在探索、开发的新能源有( )
①核能 ②柴草 ③煤炭 ④太阳能 ⑤氢能 ⑥液化石油气⑦水煤气 ⑧天然气.
①核能 ②柴草 ③煤炭 ④太阳能 ⑤氢能 ⑥液化石油气⑦水煤气 ⑧天然气.
| A、①④⑤ | B、②③⑥⑦ |
| C、③⑥⑦⑧ | D、①②④ |
下列关于粒子结构的描述不正确的是( )
| A、H2S和NH3均是价电子总数为8的极性分子 |
| B、HS-和HCl均是含一个极性键的18电子粒子 |
| C、1molD216O中含中子、质子、电子各10NA(NA代表阿伏加德罗常数的值) |
| D、CH2C12和CCl4均是四面体构型的非极性分子 |
同种元素形成的不同原子(或离子)一定具有相同的( )
| A、质量数 | B、质子数 |
| C、中子数 | D、核外电子数 |
下列有关化学用语错误的是( )
A、乙醇分子球棍模型: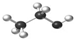 | ||
B、8个中子的碳原子的核素符号:
| ||
C、-OH的电子式: | ||
D、CH4Si的结构式: |
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A、1mol乙基中含有的电子数为17NA |
| B、标准状况下,22.4L三氯甲烷中共价键数目为4NA |
| C、1mol硫粉与足量的Cu粉共热,转移的电子数为1NA |
| D、7.8gNa2O2晶体中含有阴阳离子总数为0.4NA |
下列反应化学方程式正确的是( )
| A、CH3COOH+CH3CH2OH→CH3COOCH2CH3+H2O | ||
B、nCH3-CH=CH2
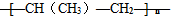 | ||
| C、CH3COO-+HCl→Cl-+CH3COOH | ||
| D、CO32-+CH3COOH→CH3COO-+CO2↑+H2O |
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液,在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液,在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: