题目内容
11.下列实验方案中,不能 达到实验目的是( )| 选项 | 实验目的 | 实验方案 |
| A | 验证盐类的水解是否是吸热反应 | 向醋酸钠溶液中滴入酚酞试液,加热观察红色是否加深 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.醋酸钠是弱酸强碱盐水解显碱性,水解过程是吸热反应;
B.稀硝酸能氧化亚铁离子生成铁离子;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.溶度积常数大的物质能转化为溶度积常数小的物质.
解答 解:A.醋酸钠是弱酸强碱盐水解显碱性,向醋酸钠溶液中滴入酚酞试液,加热后若红色加深,碱性增强,平衡正向进行证明水解过程是吸热反应,故A正确;
B.加入稀硫酸后,相当于溶液中含有硝酸,硝酸能氧化亚铁离子生成铁离子,所以干扰原溶液中铁离子的检验,故B错误;
C.将少量溴水加入KI溶液中,再加入CCl4,振荡,静置.可观察到下层液体呈紫色,说明溴和碘离子发生氧化还原反应生成碘,溴是氧化剂、碘是氧化产物,氧化剂的氧化性大于氧化产物的氧化性,所以验证Br2的氧化性强于I2,故C正确;
D.溶度积常数大的物质能转化为溶度积常数小的物质,将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色,说明氢氧化镁转化为氢氧化铁沉淀,则氢氧化镁溶解度大于氢氧化铁,故D正确;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化性强弱判断、盐类水解、离子检验、溶度积大小比较等知识点,明确实验原理及物质性质是解本题关键,注意:检验物质时要排除其它因素的干扰,易错选项是B.

练习册系列答案
相关题目
1.KNO3溶液中含杂质KCl、K2SO4和Ca(NO3)2,除去杂质所用的试剂有 ①Ba(NO3)2②K2CO3③AgNO3④HNO3,则加入试剂的正确顺序是( )
| A. | ①②③④ | B. | ②①③④ | C. | ④①③② | D. | ③①②④ |
2.某洗衣粉不仅能除去汗渍,而且有较强的除去血渍、奶渍等污物的能力,这是因为该洗衣粉中加入了( )
| A. | 食盐 | B. | 淀粉酶 | C. | 蛋白酶 | D. | 酒精 |
19.下列物质中,属于电解质的是( )
| A. | 碳酸钙 | B. | 盐酸 | C. | 铜 | D. | 酒精 |
3.分类是化学研究常用的方法,下列物质分类正确的是( )
| 选项 | 纯净物 | 酸性氧化物 | 碱性氧化物 | 酸 | 盐 |
| A | 碱石灰 | 二氧化硫 | 氧化铝 | 乙二酸 | 小苏打 |
| B | 五水硫酸铜 | 三氧化硫 | 氧化铜 | 油酸 | 苏打 |
| C | 过氧化氢 | 五氧化二磷 | 过氧化物 | 硬脂酸 | 碱式碳酸铜 |
| D | 盐酸 | 一氧化碳 | 氧化镁 | 冰醋酸 | 小苏打 |
| A. | A | B. | B | C. | C | D. | D |
20.图分别表示红磷、白磷燃烧时的能量变化,下列说法中正确的是( )
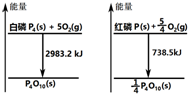

| A. | 白磷比红磷稳定 | |
| B. | 白磷燃烧产物比红磷燃烧产物稳定 | |
| C. | 1mol白磷转变为红磷放出2244.7kJ的热量 | |
| D. | 红磷燃烧的热化学方程式:4P(s)+5O2(g)→P4O10(s)+2954 kJ |
1.天然油脂结构的核心为甘油(HOCH2CHOHCH2OH),有一种瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11).该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如图所示(注:图中的反应式不完整).则下列说法不正确的是( )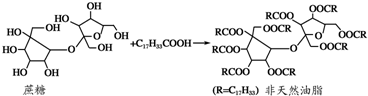

| A. | 该非天然油脂结构中含有2种官能团 | |
| B. | 油酸与蔗糖发生的反应类型属于取代反应 | |
| C. | 该非天然油脂能与氢氧化钠溶液、溴的四氯化碳溶液发生反应 | |
| D. | 蔗糖分子可以看作是两个不同的单糖分子间脱去一个水分子形成的 |
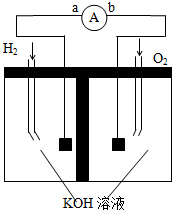 氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题
氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题