题目内容
下列说法正确的是( )
| A、物质发生化学变化时不一定都伴随能量变化 |
| B、反应热指的是反应过程中放出的热量 |
| C、在加热条件下进行的反应均为吸热反应 |
| D、相同物质的反应,当化学计量数不同时,其△H也不同 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、从化学反应的实质分析;
B、反应热可以是放热也可能是吸热;
C、反应热与反应条件无关;
D、焓变的数值与化学计量数有关.
B、反应热可以是放热也可能是吸热;
C、反应热与反应条件无关;
D、焓变的数值与化学计量数有关.
解答:
解:A、化学反应的过程是旧键断裂和新键形成的过程,断键吸收能量成键释放能量,所以任何化学反应都有能量变化,故A错误;
B、反应热是指反应过程中放出或吸收的热量,故B错误;
C、反应热与反应条件无关,故C错误;
D、△H的数值与化学计量数成正比,故D正确;
故选D.
B、反应热是指反应过程中放出或吸收的热量,故B错误;
C、反应热与反应条件无关,故C错误;
D、△H的数值与化学计量数成正比,故D正确;
故选D.
点评:本题考查了化学反应的实质、反应热、焓变与化学计量数的关系,题目难度不大.

练习册系列答案
相关题目
PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下
发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如表所示.则有关判断不正确的是( )
发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如表所示.则有关判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A、10 min内,v(Cl2)=0.04mol/(L?min) |
| B、升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 |
| C、当容器中Cl2为1.2mol时,反应达到平衡 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2mol/L |
某学生测定CuSO4?xH2O晶体的x值,数据如下(已知x的理论值为5.0):
产生误差的可能原因是( )
| 坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
| 11.70g | 20.82g | 16.02g |
| A、硫酸铜晶体中含不挥发杂质 |
| B、加热时有晶体溅出 |
| C、实验前,晶体表面有吸附水 |
| D、未做恒重操作 |
将淀粉与KI的混合液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后,取烧杯中的液体进行实验,能证明半透膜有破损的是( )
| A、加入碘水不变蓝色 |
| B、加入碘水变蓝色 |
| C、加入AgNO3溶液不产生黄色沉淀 |
| D、加入AgNO3溶液产生黄色沉淀 |
下列关于纯净物、混合物、电解质、非电解质的正确组合为( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 干冰 |
| B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
| C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
| D | 胆矾 | 水煤气 | 氯化铜 | 碳酸钠 |
| A、A | B、B | C、C | D、D |
下列物质属于糖类且属于高分子化合物的是( )
| A、蔗糖 | B、牛油 |
| C、纤维素 | D、蛋白质 |
某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是( )
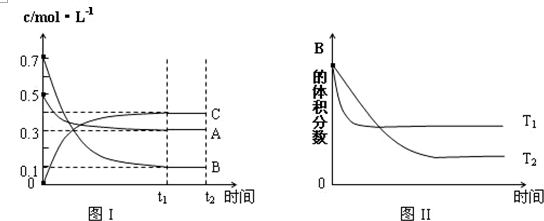

| A、该反应的热化学方程式为:A(g )+3B(g)?2C(g);△H>0 |
| B、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C、达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D、若其它条件不变,升高温度,正、逆反应速率均增大,A的转化率减小 |
下列化学用语或模型图示正确的是( )
| A、HClO的结构式:H-Cl-O |
B、Na2O2的电子式: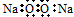 |
C、CO2的比例模型: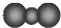 |
| D、Na原子外围电子排布式:3s1 |
下列溶液中的Cl-物质的量与100ml 1mol?L-1AlCl3溶液中Cl-相等的是( )
| A、150ml 1 mol?L-1NaCl溶液 |
| B、100ml 3mol?L-1KClO3溶液 |
| C、75ml 2 mol?L-1MgCl2溶液 |
| D、50ml 1 mol?L-1FeCl3溶液 |