题目内容
在离子晶体中正、负离子间力求尽可能多的接触,以降低体系的能量,使晶体稳定存在.已知Na+半径是Cl-的a倍,Cs+半径是Cl-的b倍,请回顾课本上NaCl和CsCl的晶胞,其晶胞边长比为 .
考点:晶胞的计算
专题:化学键与晶体结构
分析:设Cl-的半径为1,则Na+半径为a,Cs+半径为b,氯化钠的晶胞结构如图所示 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
×2(1+b),据此可以答题.
 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
| ||
| 3 |
解答:
解:设Cl-的半径为1,则Na+半径为a,Cs+半径为b,氯化钠的晶胞结构如图所示 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
×2(1+b),所以氯化钠与氯化铯的晶胞边长比为2(1+a):
×2(1+b)=
,
故答案为:
;
 ,晶胞的边长为2(1+a);氯化铯的晶胞结构为
,晶胞的边长为2(1+a);氯化铯的晶胞结构为 ,晶胞的体对角线长度为2(1+b),则晶胞的边长为
,晶胞的体对角线长度为2(1+b),则晶胞的边长为
| ||
| 3 |
| ||
| 3 |
| ||
| 1+b |
故答案为:
| ||
| 1+b |
点评:本题难度不大,解题关键在于熟悉晶胞的结构,运用几何中的有关基础知识解决问题.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、使用可再生资源、注重原子的经济性、推广利用二氧化碳与环氧丙烷生成的生物降解材料等都是绿色化学的内容 |
| B、对“地沟油”加工处理可以达到变废为宝的目的,比如对“地沟油”进行分馏可以制得汽油和煤油 |
| C、乙醇和二甲醚互为同分异构体,利用红外光谱法或核磁共振氢谱法均可鉴别两者 |
| D、绿色荧光蛋白在研究癌症发病机制的过程中应用突出,但其在酸性或碱性条件下可能会失去发光功能 |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | +1 | -4 | -2 | -1 |
| A、乙的常见氧化物只有一种 |
| B、气态氢化物稳定性:丙>丁 |
| C、丙的氧化物能与戊的氢化物的水溶液反应 |
| D、原子半径大小:戊<丙 |
下列离子方程式正确的是( )
| A、Na2S溶液中滴入酚酞呈现红色:S2-+2H2O?H2S+2OH- | ||||
B、用铜为电极电解饱和食盐水:2Cl-+2H2O
| ||||
| C、醋酸溶解含碳酸钙的水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| D、小苏打溶液中加少量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
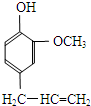 某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如右图所示,请回答:
某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如右图所示,请回答: 如图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系.其中A点表示的单质是
如图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系.其中A点表示的单质是