题目内容
已知NH3难溶于CCl4,如图所示,下列装置中,不宜用于吸收氨气的是( )
A、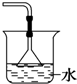 |
B、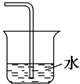 |
C、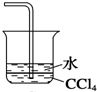 |
D、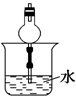 |
考点:尾气处理装置,氨的化学性质
专题:化学实验基本操作
分析:氨气极易溶于水,直接用水吸收,能够发生倒吸现象,所以吸收氨气时所选装置必须具有防止倒吸的作用,A中用倒扣的漏斗、C中四氯化碳、D中干燥管都可以起到防止倒吸的现象.
解答:
解:A.倒扣的漏斗使NH3充分吸收同时防止倒吸现象的发生,故A错误;
B.由于NH3易溶于水,可发生倒吸现象,导管不能插入液面以下,故B正确;
C.由于NH3难溶于CCl4,NH3与CCl4接触不易发生倒吸现象,能够用于吸收氨气,故C错误;
D.由于干燥管的上部大,能够防止倒吸现象的发生,故D错误;
故选B.
B.由于NH3易溶于水,可发生倒吸现象,导管不能插入液面以下,故B正确;
C.由于NH3难溶于CCl4,NH3与CCl4接触不易发生倒吸现象,能够用于吸收氨气,故C错误;
D.由于干燥管的上部大,能够防止倒吸现象的发生,故D错误;
故选B.
点评:本题考查了氨气的吸收装置,题目难度不大,注意易溶于水的气体,在尾气吸收时必须防止倒吸,要求学生掌握常见气体尾气处理方法,试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用所学知识解决实际问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
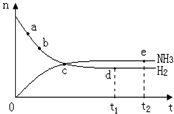 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g)
| 催化剂 |
| 高温高压 |
| A、点a的正反应速率比b点的大 |
| B、反应达到平衡时,v(N2)正=2v(NH3)逆 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点值大 |
固体碘在受热时发生升华现象,有关叙述正确的是( )
| A、碘受热升华,破坏的是分子间作用力,未破坏I-I共价键,因此未发生吸热反应 |
| B、碘受热升华,吸收热量,发生了吸热反应 |
| C、碘升华,未破坏共价键,不供应热量也能发生 |
| D、碘升华过程中,热能转变为化学能 |
砒霜中毒事件时有发生,砒霜的主要成分是三氧化二砷(As2O3),医生通常给砒霜中毒患者服用一定剂量的氧化剂解毒.下列有关叙述正确的是( )
| A、砷的+3价化合物的毒性强于+5价化合物 |
| B、砷原子最外层有3个电子 |
| C、砷化氢(AsH3)比NH3稳定 |
| D、砷酸(H3AsO4)的酸性强于磷酸 |
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂.工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)湿法制备的主要反应方程为:2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4下列有关说法不正确的是( )
| A、高铁酸钾与水反应时,水发生还原反应 |
| B、湿法中每生成1molNa2FeO4转移3mol电子 |
| C、干法中每生成1molNa2FeO4转移4mol电子 |
| D、K2FeO4处理水时,不仅能消毒杀菌,还能除去H2S、NH3等,并使悬浮杂质沉降 |
有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应.下列离子方程式中,只能表示一个化学反应的是( )
①Fe+Cu2+═Fe2++Cu
②Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
③Cl2+H2O═H++Cl-+HClO
④CO32-+2H+═CO2↑+H2O
⑤Ag++Cl-═AgCl↓
①Fe+Cu2+═Fe2++Cu
②Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O
③Cl2+H2O═H++Cl-+HClO
④CO32-+2H+═CO2↑+H2O
⑤Ag++Cl-═AgCl↓
| A、只有③ | B、②③ | C、③⑤ | D、①④ |
次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐(不存在酸式盐).下列叙述中正确的是( )
| A、次磷酸(H3PO2)是三元酸 |
| B、H3PO2中磷为+1价 |
| C、NaH2PO2溶液呈酸性 |
| D、次磷酸根离子为-3价 |
水热法制备Fe3O4纳米颗粒的化学方程式为:3Fe++2S2O
+O2+4OH-=Fe3O4+X+2H2O.下列有关说法不正确的是( )
2- 3 |
| A、上式中的X为S4O62- |
| B、该反应中的还原剂为Fe2+和S2O32- |
| C、当生成1 mol Fe3O4时,转移电子的物质的量为4 mol |
| D、当3 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1 mol |
