题目内容
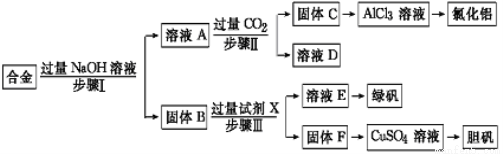
(12分)为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
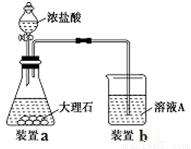
(3)进行步骤Ⅱ时,该小组用如下图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
(1)2Al+2OH—+2H2O=2AlO2-+3H2↑(2分)(2)稀硫酸或H2SO4(2分) 过滤(2分)
(3)在装置Ⅰ、Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶(2分)
(4)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O(2分)
途径②最佳,理由是原料利用率高,环境污染小(2分)
【解析】
试题分析:(1)在合金中含有铝、铁和铜,向其中加入过量的NaOH溶液,其中的Al会发生反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,步骤Ⅰ反应的离子方程式是:2Al+2OH-+2H2O=2AlO2-+3H2↑,(2)而Fe、Cu不能发生反应,过滤出来;在固体B中含有Fe、Cu,向其中加入过量的硫酸,由于Fe的活动性在金属活动性顺序表H前边,而Cu位于H的后边,所以Fe发生反应产生FeSO4,而Cu仍然是固体,将二者通过过滤分离开来,滤液蒸发浓缩、冷却结晶,就得到绿矾;再向固体Cu中加入浓硫酸并加热,发生氧化还原反应产生CuSO4,将该溶液蒸发浓缩冷却结晶,就得到胆矾。向含有NaAlO2的滤液中通入过量的CO2气体,会产生Al(OH)3沉淀和NaHCO3溶液,将沉淀和溶液通过过滤分离开,将沉淀沉淀后用适量的盐酸溶解得到AlCl3溶液,最后在HCl的气氛中加热蒸发水分得到固体AlCl3。所以X是稀硫酸;步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是过滤;(3)由于盐酸有挥发性,在制取的CO2气体中含有杂质HCl,所以直接进行步骤Ⅱ时制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,应该先将杂质HCl除去,可采取的改进措施是在装置Ⅰ、Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶;(4)在途径①中,Cu与稀硫酸、稀硝酸的混合物反应的离子方程式是:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;在途径①中会产生有毒气体NO,不环保;在途径②中,Cu与氧气加热产生CuO,再用酸溶解,得到硫酸铜,不仅无污染,而且原料的利用率也高;在途径③中发生反应:Cu+2H2SO4(浓) 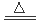 CuSO4+SO2↑+2H2O,会产生大气污染物SO2,而且原料的利用率也降低,因此三种方法比较,最好的是方法②。
CuSO4+SO2↑+2H2O,会产生大气污染物SO2,而且原料的利用率也降低,因此三种方法比较,最好的是方法②。
考点:考查物质的综合利用的知识,主要包括方案的设计、物质的选择、方法的比较、方程式的书写。

 阅读快车系列答案
阅读快车系列答案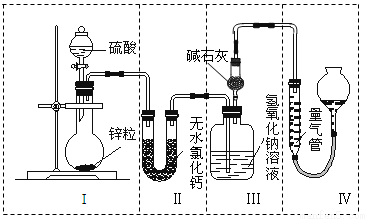
 [Cu(NH3)3CO]Ac 。完成下列填空:
[Cu(NH3)3CO]Ac 。完成下列填空: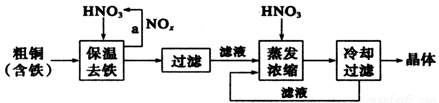

 OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。
OH—+H3O+, 则液态NH3电离的方程式是 ,液态N2O4电离得到电子数相差18的阴阳离子,因此可用Cu与液态N2O4反应制备无水硝酸铜,其反应的化学方程式是 。 BCl3空间形状为 (用文字描述)。
BCl3空间形状为 (用文字描述)。 键数目为 。
键数目为 。