题目内容
3.在如图所示的微粒中,结合电子能力最强的是( )| A. | 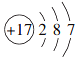 | B. | 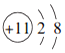 | C. |  | D. |  |
分析 A.为氯原子;B.为钠离子;C.为氟原子;D.为氧离子.结合电子能力最强的为得电子能力最强的微粒,同一主族元素,元素的金属性随着原子序数增大而增大,元素的非金属性随着原子序数增大而减弱,元素的非金属性越强,其得电子能力越强,据此分析解答.
解答 解:A.图示为氯原子,易得一个电子形成氯离子;
B.图示为钠离子,已经达到稳定结构,难得电子;
C.图示为氟原子,易得一个电子形成最外层8电子稳定结构的氟离子;
D.图示为氧离子,已经达到稳定结构,难得电子;因此只要比较氟、氯的非金属性,
同一主族元素,元素的非金属性随着原子序数增大而减小,元素的非金属性越强,其得电子能力越强,氟、氯两种元素处于同一主族,氟在第二周期,氯在第三周期,非金属性强弱顺序是F>Cl,所以得电子能力最强的是F元素,
故选C.
点评 本题考查同一主族元素性质递变规律,侧重考查学生对元素周期律的综合应用,明确元素周期律内涵即可解答,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
14.有机物X是合成二氢荆芥内酯的重要原料,其结构简式为 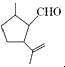 ,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )
,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )
 ,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )
,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )| A. | 先加酸性高锰酸钾溶液,后加银氨溶液,加热 | |
| B. | 先加溴水,后加酸性高锰酸钾溶液 | |
| C. | 先加银氨溶液,加热,再加入溴水 | |
| D. | 先加入新制氢氧化铜悬浊液,加热,取清液酸化后再加溴水 |
11.NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.5mol C4H10中含有的共价键数为6.5NA | |
| B. | 3.4 g羟基和3.4 g氢氧根均含有2NA个电子 | |
| C. | 1L0.1 mol•L-1CH3COOH溶液中含有的氧原子数为0.2NA | |
| D. | 标准状况下,22.4L由CHCl3和CH2Cl2组成的混合物中含有的分子数目为NA |
18.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 42gC3H6中含有的共用电子对数目为8NA | |
| B. | 由6gCaCO3和5gKHCO3组成的混合物中含有的碳原子数为0.11NA | |
| C. | 标准状况下,22.4L氯气和56g铁充分反应,转移的电子数为3NA | |
| D. | 1L0.01mol•L-1Kal(SO4)2溶液中含有的阳离子数为0.02NA |
8.下列各组微粒具有相同的质子数和电子数的是( )
| A. | OH-、H2O | B. | NH3、NH4+ | C. | H3O+、NH2- | D. | HC1、H2S |
12.下列叙述不正确的是( )
①热稳定性:H2O>HF>H2S
②熔点:Li>Na>K
③第I A、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3<PH3<AsH3.
①热稳定性:H2O>HF>H2S
②熔点:Li>Na>K
③第I A、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3<PH3<AsH3.
| A. | ①②⑤ | B. | ①③④ | C. | ①②③⑤ | D. | ①③⑤ |
13.表为元素周期表的一部分,X、Y、Z、R为短周期元素,其中Y元素的原子最外层电子数是其内层电子数的3倍,下列说法正确的是( )
| X | Y | |
| Z | ′ | R |
| W |
| A. | 原子半径大小关系为:R>Y>X | |
| B. | X有多种同素异形体,而Y不存在同素异形体 | |
| C. | 根据元素周期律t可以推测W元素的单质具有半导体特性,W2Y3具有氧化性和还原性 | |
| D. | 氢化物熔沸点:H2R>H2Y |

 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$ +H2O.
+H2O.