题目内容
 实验室制得气体中常含有杂质,影响其性质检验.如图A为除杂装置,B为性质检验装置,完成下列表格:
实验室制得气体中常含有杂质,影响其性质检验.如图A为除杂装置,B为性质检验装置,完成下列表格:| 序号 | 气体 | 反应原理 | A中试剂 |
| ① | 乙烯 | 溴乙烷和NaOH的醇溶液加热 | |
| ② | 乙烯 | 无水乙醇在浓硫酸的作用下加热至170℃反应的化学方程式是 | NaOH溶液 |
| ③ | 乙炔 | 电石与饱和食盐水反应 |
考点:物质分离、提纯的实验方案设计,实验装置综合
专题:实验设计题
分析:①乙烯混有乙醇,可用水除杂;
②无水乙醇在浓硫酸的作用下加热至170℃反应,生成乙烯和水;
③乙炔中混有硫化氢气体,可用硫酸铜除杂.
②无水乙醇在浓硫酸的作用下加热至170℃反应,生成乙烯和水;
③乙炔中混有硫化氢气体,可用硫酸铜除杂.
解答:
解:①乙醇易挥发,且易溶于水,乙烯混有乙醇,可用水除杂,故答案为:水;
②无水乙醇在浓硫酸的作用下加热至170℃反应,生成乙烯和水,反应的方程式为CH3CH2OH
CH2=CH2↑+H2O,故答案为:CH3CH2OH
CH2=CH2↑+H2O;
③乙炔中混有硫化氢气体,可用硫酸铜除杂,生成CuS沉淀,故答案为:CuSO4溶液.
②无水乙醇在浓硫酸的作用下加热至170℃反应,生成乙烯和水,反应的方程式为CH3CH2OH
| 浓硫酸 |
| 170℃ |
| 浓硫酸 |
| 170℃ |
③乙炔中混有硫化氢气体,可用硫酸铜除杂,生成CuS沉淀,故答案为:CuSO4溶液.
点评:本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理以及物质的性质,难度不大.

练习册系列答案
相关题目
下列实验对应的离子方程式正确的是( )
| A、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D、用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++7H2O2═2Mn2++6O2↑+10H2O |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、气态氢化物的稳定性:HnX 强于HmY |
| B、X和Y形成化合物时,X显负价,Y显正价 |
| C、第一电离能一定是:Y小于X |
| D、最高价含氧酸的酸性:X>Y |
某学生在实验室制取乙酸乙酯(反应温度80℃左右)和乙酸丁酯(反应温度115~125℃),现有两套实验装置图Ⅰ和图Ⅱ.下列说法错误的是( )
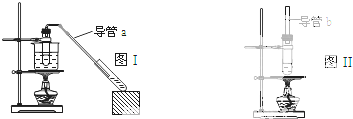

| A、制乙酸乙酯用图I装置,制乙酸丁酯用图II 装置 |
| B、导管a和导管b的作用都是冷凝回流 |
| C、都可用Na2CO3 溶液来洗去酯中的酸和醇 |
| D、加入过量的乙酸可以提高醇的转化率 |
已知某元素原子的各级电离能( kJ?mol-1)数值如下表,则该原子最外层的电子数为( )
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 577 | 1820 | 2740 | 11600 | 14800 | 18400 | 23400 |
| A、1 | B、3 | C、5 | D、7 |
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
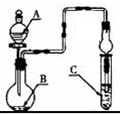

| A、若A为浓硫酸,B为铜,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛CaCl2溶液,则C中溶液变浑浊 |
| C、若A为浓盐酸,B为MnO2,C中盛KI-淀粉溶液,则C中溶液变蓝 |
| D、若A为水,B为Na2O2固体,C中盛氢硫酸溶液,则C中溶液变浑浊 |
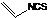 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3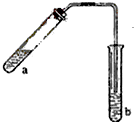 哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: