题目内容
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
(14分)(1)第三周期第ⅢA族(2分)
(2)①4Al+3O2+6H2O=4Al(OH)3 (2分) ②增强溶液的导电能力(2分)
③I-+3H2O-6e-=IO3-+6H+ (2分) ④2.7g (2分)
(3) ①
 (2分)②Al2O3+3C+3Cl2
(2分)②Al2O3+3C+3Cl2
 2AlCl3+3CO. (2分)
2AlCl3+3CO. (2分)
【解析】
试题分析:(1)13号元素铝元素原子的核外电子排布是2、8、3,其在元素周期表中的位置是第三周期第ⅢA族;(2)在负极发生反应:4Al-12e-=4Al3+;在正极发生反应:3O2+6H2O+12e-+4Al3+=4Al(OH)3。总反应方程式是4Al+3O2+6H2O=4Al(OH)3。②电池中NaCl的作用是电解质,提供自由移动的离子,增强溶液的导电能力;③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料),溶液中的阴离子放电,由于放电能力:I->OH-,所以I-在阳极放电,阳极的电极反应式为I-+3H2O-6e-=IO3-+6H+;④NaCl溶液电解的方程式是:2NaCl+2H2O Cl2↑+H2↑+2NaOH,每产生2mol的NaOH,转移2mol的电子,n(NaOH)= 0.3 mol/L×0.5L=0.15mol,铝一空气电池的效率为50%,所以转移电子的物质的量是0.15mol÷50%=0.30mol,Al是+3价的金属,所以反应消耗的Al的物质的量是0.30mol÷3=0.10mol,其质量是m(Al)= 0.10mol×27g/mol=2.7g;(3)①氯化铝在加热条件下易升华,说明该物质是分子晶体,在气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为
Cl2↑+H2↑+2NaOH,每产生2mol的NaOH,转移2mol的电子,n(NaOH)= 0.3 mol/L×0.5L=0.15mol,铝一空气电池的效率为50%,所以转移电子的物质的量是0.15mol÷50%=0.30mol,Al是+3价的金属,所以反应消耗的Al的物质的量是0.30mol÷3=0.10mol,其质量是m(Al)= 0.10mol×27g/mol=2.7g;(3)①氯化铝在加热条件下易升华,说明该物质是分子晶体,在气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 ;②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,根据元素守恒及电子守恒可得该反应的化学方程式是Al2O3+3C+3Cl2
;②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,根据元素守恒及电子守恒可得该反应的化学方程式是Al2O3+3C+3Cl2
 2AlCl3+3CO。
2AlCl3+3CO。
考点:考查元素在周期表中的位置、原电池、电解池反应原理及应用、物质结构式、反应方程式的书写的知识。

下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是
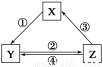
选项 | X | Y | Z | 箭头上所标数字的反应条件 |
A | CaO | Ca(OH)2 | CaCO3 | ①常温遇水 |
B | AlCl3 | NaAlO2 | Al(OH)3 | ②通入CO2 |
C | Na2CO3 | NaOH | NaHCO3 | ④过量Ca(OH)2溶液 |
D | Cl2 | Ca(ClO)2 | HClO | ③加浓盐酸 |
X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20,下列判断正确的是
W | X | Y |
Z |
A.四种元素的原子半径:rZ>rX>rY>rW
B.四种元素形成的单质最多有6种
C.四种元素均可与氢元素形成电子总数为18的分子
D.四种元素中,Z的最高价氧化物对应的水化物酸性最强








 单体的结构简式为_________。用类似反应①的方法,利用丙炔与合适的原料可以合成该单体,化学方程式为________。
单体的结构简式为_________。用类似反应①的方法,利用丙炔与合适的原料可以合成该单体,化学方程式为________。