题目内容
11.下列关于硅的化学性质的叙述,正确的是( )| A. | 常温时不和任何酸反应 | B. | 常温时可和强碱溶液反应 | ||
| C. | 单质硅比碳的还原性弱 | D. | 单质硅比碳的氧化性强 |
分析 A、硅可以和HF酸之间反应;
B、硅常温时可和强碱溶液反应生成硅酸盐和水;
C、同主族元素,从上到下,单质的还原性逐渐增强;
D、同主族元素,从上到下,单质的氧化性逐渐减弱.
解答 解:A、常温时硅可以和HF酸之间反应,故A错误;
B、硅常温时可和强碱溶液反应生成硅酸盐和水,故B正确;
C、同主族元素,从上到下,单质的还原性逐渐增强,单质硅比碳的还原性强,故C错误;
D、同主族元素,从上到下,单质的氧化性逐渐减弱,单质硅比碳的氧化性弱,故D错误.
故选B.
点评 本题考查学生物质的性质以及元素周期律的有关知识,属于综合知识的考查,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.溶液中可以大量共存的一组离子是( )
| A. | Al3+、Na+、OH-、Cl- | B. | H+、AlO2-、Na+、SO42- | ||
| C. | Mg2+、AlO2-、Al3+、NO3- | D. | OH-、AlO2-、K+、Na+ |
2.在密闭容器中把CO和H2O的混合物加热到800℃,有下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),且平衡常数K=1.若在2L的密闭容器中充入1mol CO和1mol H2O相互混合并加热到800℃,则CO的转化率为( )
| A. | 40% | B. | 50% | C. | 60% | D. | 83.3% |
19.元素X与元素Y在周期表中位于相邻的两个周期,X与Y两原子核外电子数之和为19,Y原子核内质子数比X多3个.下列描述正确的是( )
| A. | X和Y都是性质活泼的元素,在自然界中只能以化合态存在 | |
| B. | X和Y形成的化合物的化学式只能为Y2X2 | |
| C. | X的化合物种类比Y的化合物种类多 | |
| D. | Y能置换酸中氢放出氢气,但不能置换盐中的金属 |
6.1mol某烃能与2mol HCl完全加成,其产物最多能被8mol Cl2完全取代,则原烃可为( )
| A. | 乙炔 | B. | 1-丁炔 | C. | 1-丙炔 | D. | 环丁烯 |
16.下列说法正确的是( )
| A. | 用 HNO2溶液作导电性实验,灯光较暗,说明 HNO2是弱电解质 | |
| B. | NaCl 溶液和 CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| C. | 25℃时,用醋酸溶液中和等浓度 NaOH 溶液至 pH=7,VCH3COOH<VNaOH | |
| D. | AgCl 易转化为 AgI 沉淀且 Ksp(AgX)=[Ag+]•[X-],故 Ksp(AgI)<Ksp(AgCl) |
3.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | 使甲基橙呈红色的溶液:NO3-、Ba2+、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | pH=12的溶液:CO32-、Cl-、K+、F- |
1.某小组为研究电化学原理,设计如图装置,下列叙述不正确的是( )
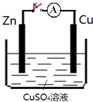

| A. | K打开,Zn片上会有金属铜析出 | |
| B. | 无论K是否闭合,锌片均会溶解,溶液均从蓝色逐渐变浅 | |
| C. | K闭合时,SO42-向铜电极移动 | |
| D. | K闭合时,电子从负极Zn流向正极 Cu,再从溶液中回到负极Zn |
 ;
;