题目内容
17.室温下,在一个无色透明恒容的密闭容器中存在如下平衡体系:2NO2 (红棕色,g)?N2O4 (无色,g)△H<0.现将该容器浸入冰水中,则正确现象是( )| A. | 气体颜色变深 | B. | 气体颜色不变 | C. | 气体颜色变浅 | D. | 先变深后变浅 |
分析 在恒容密闭容器中,可逆反应达到平衡后,无色透明恒容的密闭容器中存在如下平衡体系:2NO2 (红棕色,g)?N2O4 (无色,g)△H<0,现将该容器浸入冰水中,平衡向放热方向移动.
解答 解:平衡体系:2NO2 (红棕色,g)?N2O4 (无色,g)△H<0,反应是放热反应,现将该容器浸入冰水中,温度降低平衡向放热方向移动.所以平衡正向进行气体颜色变浅,
故选C.
点评 本题考查了温度对化学平衡的影响,平衡移动原理是解题关键,注意反应特征是放热反应,二氧化氮为红棕色气体,四氧化二氮为无色,题目较简单.

练习册系列答案
相关题目
8.下列关于有机物的叙述正确的是( )
| A. | 糖类、油脂和蛋白质均为高分子化合物 | |
| B. | 利用溴的四氯化碳溶液可除去甲烷中的乙烯 | |
| C. | 煤中含有苯、甲苯等,可通过煤的干馏制取 | |
| D. | 苯滴入溴水中振荡后水层接近无色,因为发生了加成反应 |
5.下列关于有机物的叙述正确的是( )
| A. | 1,2-二氯乙烷在NaOH水溶液中加热发生消去反应得到乙炔 | |
| B. | 石油液化气、汽油和石蜡的主要成分都是碳氢化合物 | |
| C. | 除去电石和水反应产生的乙炔中杂质气体,可用稀硫酸洗气 | |
| D. | 由丙烯酸甲酯CH2=CHCOOCH3合成的聚合物为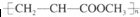 |
12.下列对碱性锌锰电池的叙述不 正确的是( )
| A. | 锌是正极,MnO2是负极 | |
| B. | 电解质是KOH溶液 | |
| C. | 锌发生氧化反应,MnO2发生还原反应 | |
| D. | 它的能量和储存时间比普通锌锰电池高 |
2. “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
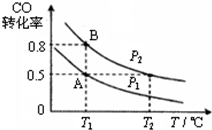
(1)向体积为 2L的密闭容器中充入1mol CO和2mol H2,在一定条件下发生如下反应:CO(g)+2H2(g)?CH3OH(g).经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如图所示.请回答:
①p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为$\frac{0.5}{t}$mol•L-1•s-1
②图中压强p1< 压强p2.(填“>”、“<”或“=”)
(2)一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
①容器I中反应达到平衡所需时间比容器Ⅲ中的短(填“长”、“短”或“相等”)
②达到平衡时,容器I中的CH3OH的体积分数相等(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数.
③若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行(填“正反应”、“逆反应”或“不移动”).
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).若反应在恒容绝热(不
与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高.
则升高温度,该反应的平衡常数将减小(填“增大”“减小”或“不变”).
 “C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.
“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义.(1)向体积为 2L的密闭容器中充入1mol CO和2mol H2,在一定条件下发生如下反应:CO(g)+2H2(g)?CH3OH(g).经过t秒达到平衡,平衡时CO的转化率与温度、压强的关系如图所示.请回答:
①p1、T1℃时,从开始到平衡的过程中,用H2表示的平均反应速率为$\frac{0.5}{t}$mol•L-1•s-1
②图中压强p1< 压强p2.(填“>”、“<”或“=”)
(2)一定温度下,在三个体积均为 1.0L的恒容密闭容器中发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)
| 容器 编号 | 温度(℃) | 起始的物质的量(mol) | 平衡的物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
②达到平衡时,容器I中的CH3OH的体积分数相等(填“大于”、“小于”或“相等”)容器Ⅱ中的CH3OH的体积分数.
③若起始时向容器I中充入CH3OH 0.1mol、CH3OCH30.15mol和H2O 0.10mol,则反应将向正反应方向进行(填“正反应”、“逆反应”或“不移动”).
(3)一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).若反应在恒容绝热(不
与外界交换能量)条件下进行,按下表数据投料,反应达到平衡状态,测得体系压强升高.
| 物质 | CO2 | H2 | CH3OH | H2O |
| 起始投料/mol | 1 | 3 | 2 | 0 |
6.下列溶液或浊液中,关于离子浓度的说法正确的是( )
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值增大 | |
| B. | 浓度均为0.1 mol•L-1的Na2CO3、NaHCO3混合溶液中:c(CO32-)>c(HCO3-),且2c(Na+)=3c(H2CO3)+3c(HCO3-)+3c(CO32-) | |
| C. | 常温下0.4 mol•L-1 HB溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-) | |
| D. | 假设HClO的电离平衡常数为Ka,碳酸的电离常数分别记为:Ka1和Ka2,已知:Ka1>Ka>Ka2,则发生反应:2NaClO+CO2(少量)+H2O═Na2CO3+2HClO |
7.常温下,一定浓度的某溶液,由水电离出的 c(OH-)=10-4mol•L-1,则该溶液中的溶质可能是( )
| A. | NaOH | B. | H2SO4 | C. | CH3COONa | D. | KCl |