题目内容
10.化学反应可以从不同的角度进行分析,以下观点中正确的是( )| A. | 放热反应在常温下均能自发进行 | |
| B. | 原电池工作时所发生的反应一定有氧化还原反应 | |
| C. | 加热时,化学反应只向吸热反应方向进行 | |
| D. | 化学平衡常数的表达式与化学反应方程式的书写无关 |
分析 A.只有持续加热才反应的,一般为吸热反应,反之,一般为放热反应;
B.原电池工作时,是将化学能转化为电能;
C.加热时,化学反应不只向吸热反应方向进行;
D.化学平衡常数的大小只与温度有关,化学平衡常数的表达式与化学反应方程式的书写有关.
解答 解:A.放热反应是指:反应物的总能量大于生成物的总能量,与常温下能自发进行无关,如:碳在空气中燃烧,须加热达到碳的着火点才可进行,故A错误;
B.原电池工作时,是将化学能转化电能,有电流产生,则有电子的定向移动,所以所发生的反应一定有氧化还原反应,故B正确;
C.加热时,提供能量,无论是吸热反应,还是放热反应,反应速率都要加快,故C错误;
D.化学平衡常数的表达式为:化学平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$,与化学反应方程式的书写有关,故D错误;
故选B.
点评 本题主要考查基础知识的辨析,主要是化学反应能量变化,反应自发进行的判断依据,结合题意,根据所学知识,注重知识的内涵和外延,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
1.KNO3溶液中含杂质KCl、K2SO4和Ca(NO3)2,除去杂质所用的试剂有 ①Ba(NO3)2②K2CO3③AgNO3④HNO3,则加入试剂的正确顺序是( )
| A. | ①②③④ | B. | ②①③④ | C. | ④①③② | D. | ③①②④ |
18.化学与生产、生活、社会密切相关,下列说法正确的是( )
| A. | 绚丽缤纷的烟花中添加了含钾、钠、铁、铜等金属元素的化合物 | |
| B. | 明矾和漂白粉常用于自来水的净化,且原理相同 | |
| C. | 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 | |
| D. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 |
5.某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化.
(1)该同学最初的实验操作和现象等如表:
(2)该同学分析了导致实验Ⅱ现象的可能原因,并对实验方案进行了改进.改进后的实验操作和现象等如表:
(3)上述实验表明,Fe3+有可能与I-发生反应.进一步查阅资料知,反应物的物质的量相同.该同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变红的原因,认为Fe3+与I-反应的离子方程式应写为2Fe3++2I-?2Fe2++I2
(4)该同学认为需要进一步设计实验证明根据实验Ⅲ中现象得出的结论.请填补表中的实验内容.
(1)该同学最初的实验操作和现象等如表:
| 编号 | 操作 | 现象等 |
| Ⅰ | 先向2mL 0.1mol/L FeC12溶液中滴加KSCN溶液,再滴加新制氯水 | ①滴加KSCN溶液后,溶液无明显变化;滴加新制氯水后,溶液变变成红色 ②FeC12溶液与新制氯水反应的离子方程式2Fe2++Cl2═2Fe3++2Cl- |
| Ⅱ | 先向2mL 0.1mol/L FeC13溶液中滴加KSCN溶液,再滴加0.1mol/L KI溶液 | 滴加KSCN溶液后,溶液变红色;滴加KI溶液后,红色无明显变化 |
| 编号 | 操作 | 现象等 |
| Ⅲ | 先向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeC13溶液,再滴加KSCN溶液 | 滴加FeC13溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变为红色.根据实验现象可以推测出Fe3+有可能与I-发生了氧化还原反应. |
(4)该同学认为需要进一步设计实验证明根据实验Ⅲ中现象得出的结论.请填补表中的实验内容.
| 编号 | 操作 | 现象及结论 |
| Ⅳ | 向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeC13溶液,再滴加①再滴加淀粉溶液(或CCl4;或铁氰化钾溶液) | 现象:溶液变蓝. 结论:Fe3+能与I-发生氧化还原反应生成②I2,③Fe2+ |
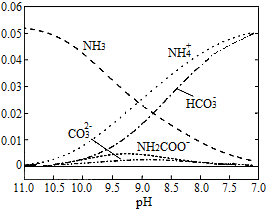
15.40℃时,在氨一水体系中不断通入C02,各种离子的变化趋势如图所示:
 ,
,
下列说法不正确的是( )
 ,
,下列说法不正确的是( )
| A. | 在pH=8.0 时,c(NH4+)>c(HCO3-)>c(NH2COO-)=c(CO32-) | |
| B. | 随着C02的不断通入,Kw不变,但是水的电离受到促进 | |
| C. | 在溶液中pH不断降低的过程中,最终产物中含有NH2COO- | |
| D. | D、随着C02的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}{H}_{2}O)}$ 不断减小 |
2.某洗衣粉不仅能除去汗渍,而且有较强的除去血渍、奶渍等污物的能力,这是因为该洗衣粉中加入了( )
| A. | 食盐 | B. | 淀粉酶 | C. | 蛋白酶 | D. | 酒精 |
19.下列物质中,属于电解质的是( )
| A. | 碳酸钙 | B. | 盐酸 | C. | 铜 | D. | 酒精 |
20.图分别表示红磷、白磷燃烧时的能量变化,下列说法中正确的是( )
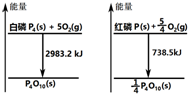

| A. | 白磷比红磷稳定 | |
| B. | 白磷燃烧产物比红磷燃烧产物稳定 | |
| C. | 1mol白磷转变为红磷放出2244.7kJ的热量 | |
| D. | 红磷燃烧的热化学方程式:4P(s)+5O2(g)→P4O10(s)+2954 kJ |