题目内容
9.下列能够说明醋酸是弱酸的是( )| A. | 醋酸能与水以任意比例混溶 | B. | 醋酸能与碳酸钠反应 | ||
| C. | 醋酸能使紫色石蕊试液变红色 | D. | 0.1mol.L-1醋酸溶液pH=3 |
分析 证明CH3COOH为弱酸,可从以下角度判断:①等浓度的HCl、CH3COOH导电能力;②比较二者的电离程度,判断是否完全电离;③判断是否存在电离平衡;④比较二者对应的盐溶液的酸碱性,⑤一定浓度的酸溶液PH等.
解答 解:A.醋酸与水能以任意比混溶,只能说明醋酸是可溶性物质,不能说明醋酸的电离程度,所以不能说明醋酸是弱电解质,故A错误;
B.醋酸和碳酸钠反应生成二氧化碳,说明醋酸的酸性比碳酸强,但不能说明醋酸是弱电解质,故B错误;
C.能使紫色石蕊试液变红是酸的通性,醋酸、盐酸都可以变红色,不能说明醋酸是否完全电离,故C错误;
D.0.1mol/L的醋酸的pH值约为3,说明醋酸部分电离为弱酸,若为强酸PH=1,故D正确;
故选D.
点评 本题注意把握判断酸性强弱的角度,从弱电解质的电离平衡的角度分析,注意电解质的强弱是根据其电离程度划分的,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.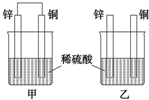 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
①两烧杯中铜片表面均无气泡产生
②甲中铜片是正极,乙中铜片是负极
③两烧杯中溶液的c(H+)均减小
④产生气泡的速率甲比乙慢
⑤甲中SO${\;}_{4}^{2-}$向Zn片移动,H+向Cu片移动
⑥乙中电流从Cu片流向Zn片
⑦甲、乙两烧杯中Cu片的质量均不变.
 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )①两烧杯中铜片表面均无气泡产生
②甲中铜片是正极,乙中铜片是负极
③两烧杯中溶液的c(H+)均减小
④产生气泡的速率甲比乙慢
⑤甲中SO${\;}_{4}^{2-}$向Zn片移动,H+向Cu片移动
⑥乙中电流从Cu片流向Zn片
⑦甲、乙两烧杯中Cu片的质量均不变.
| A. | ①②③ | B. | ③⑤⑦ | C. | ④⑤⑥ | D. | ②③④⑤⑦ |
20.关于如图所示化合物的说法正确的是( )
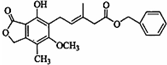

| A. | 分子中所有的原子共平面 | |
| B. | 既可以使溴水褪色.又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 1 mol该化合物最多可以与9mol H2发生加成反应 | |
| D. | 该物质能发生取代反应、氧化反应、加成反应 |
17.下列各组顺序的排列不正确的是( )
| A. | 酸性强弱:HClO4>H2SO4>H3PO4 | B. | 离子半径:Na+>Mg2+>Al3+>F- | ||
| C. | 热稳定性:H2S>PH3>SiH4>HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |
4.以下除杂方案不正确的是( )
| A. | Cl2中混有HCl,可依次通入盛有饱和食盐水、浓H2SO4的洗气瓶 | |
| B. | NH4Cl 溶液中混有Fe3+,可加入NaOH溶液后过滤 | |
| C. | CO中混有CO2,可依次通入盛NaOH 溶液、浓 H2SO4的洗气瓶 | |
| D. | Na2CO3固体中混有NaHCO3,可用灼烧的方法除尽 |
14.下列实验能达到预期目的是( )
| A. | 用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 | |
| B. | 用食醋和澄清石灰水验证蛋壳中含碳酸盐 | |
| C. | 直接往淀粉水解液中滴入银氨溶液可产生银镜 | |
| D. | 用分液漏斗分离溴和苯 |
18.Na3N是离子化合物,它和水作用可产生NH3.下列叙述正确的是( )
| A. | Na3N与盐酸反应生成的都是盐 | |
| B. | Na+和N3-的电子层结构不相同 | |
| C. | Na+的半径大于N3-的半径 | |
| D. | 在Na3N与水的反应中,Na3N做还原剂 |
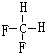 和
和